
МУК 4.2.1018-01 Санитарно-микробиологический анализ питьевой воды (с Изменением N 1)
МУК 4.2.1018-01
МЕТОДИЧЕСКИЕ УКАЗАНИЯ
4.2. Методы контроля.
Биологические и микробиологические факторы
САНИТАРНО-МИКРОБИОЛОГИЧЕСКИЙ АНАЛИЗ ПИТЬЕВОЙ ВОДЫ
Дата введения 2001-07-01
1. РАЗРАБОТАНЫ НИИ экологии человека и гигиены окружающей среды им. А.Н.Сысина РАМН (Недачин А.Е., Доскина Т.В., Дмитриева Р.А., Тишкова Н.Ю., Сидоренко С.Г.), Федеральным научным центром гигиены им. Ф.Ф.Эрисмана Минздрава России (Трухина Г.М., Мойсеенко Н.Н., Сарафанюк Е.В.), Аналитическим центром контроля качества воды "Роса" (Кашкарова Г.П.), Федеральным центром госсанэпиднадзора Минздрава России (Кривопалова Н.С., Сорокина Р.С.), Центром госсанэпиднадзора в г.Москве (Салова Н.Я., Малышева З.Г., Кожевникова Н.А.), Центром госсанэпиднадзора в Московской области (Козлова А.Т.), Московским НИИ генетики (Бовыкина Н.М.), НИИ коммунального водоснабжения и очистки воды (Русанова Н.А.), Российской медицинской академией последипломного образования (Власова И.В.), Российским государственным медицинским университетом (Пивоваров Ю.П.).
2. УТВЕРЖДЕНЫ Главным государственным санитарным врачом Российской Федерации - Первым заместителем министра здравоохранения Российской Федерации 9 февраля 2001 г.
3. С момента ввода данных методических указаний считаются утратившими силу методические указания МУК 4.2.671-97 "Методы санитарно-микробиологического анализа питьевой воды" и Информационно-методическое письмо Департамента государственного санитарно-эпидемиологического надзора Министерства здравоохранения Российской Федерации N 1100/1670-98-111 "О дополнительных мерах по осуществлению контроля качества питьевой воды по микробиологическим и паразитологическим показателям".
4. ВВЕДЕНЫ ВПЕРВЫЕ.
ВНЕСЕНО Изменение N 1, утвержденное и введенное в действие Главным государственным санитарным врачом Российской Федерации 23 декабря 2010 года
Изменение N 1 внесено изготовителем базы данных по тексту М.: Федеральный центр гигиены и эпидемиологии Роспотребнадзора, 2011 год
1. Область применения
1.1. Настоящие методические указания устанавливают методы санитарно-микробиологического контроля качества питьевой воды в отношении ее эпидемической безопасности по показателям СанПиН 2.1.4.559-96 "Питьевая вода. Гигиенические требования к качеству воды централизованных систем питьевого водоснабжения. Контроль качества".
1.2. Методические указания предназначены для лабораторий организаций, предприятий и иных хозяйственных субъектов, осуществляющих производственный контроль, а также органов санитарно-эпидемиологической службы, обеспечивающих государственный и ведомственный санитарно-эпидемиологический надзор за качеством питьевой воды централизованных систем питьевого водоснабжения.
2. Нормативные ссылки
3. Отбор, хранение и транспортирование проб
3.1. Общие требования к отбору проб
3.1.1. Отбор проб производит специалист после прохождения инструктажа по технике выполнения отбора проб для микробиологического анализа.
3.1.2. Для отбора проб воды используют специально предназначенную для этих целей одноразовую посуду или емкости многократного применения, изготовленные из материалов, не влияющих на жизнедеятельность микроорганизмов.
3.1.3. Емкости должны быть оснащены плотно закрывающимися пробками (силиконовыми, резиновыми или из других материалов) и защитным колпачком (из алюминиевой фольги, плотной бумаги). Многоразовая посуда, в т.ч. пробки, должна выдерживать стерилизацию сухим жаром или автоклавированием.
3.1.4. При отборе проб в одной и той же точке для различных целей первыми отбирают пробы для бактериологических исследований. Если отбирают воду после обеззараживания химическими реагентами, то для нейтрализации остаточного количества дезинфектанта в емкость, предназначенную для отбора проб, вносят до стерилизации натрий серноватисто-кислый в виде кристаллов из расчета 10 мг на 500 мл воды.
3.1.5. Пробу отбирают в стерильные емкости. Емкость открывают непосредственно перед отбором, удаляя пробку вместе со стерильным колпачком. Во время отбора пробка и края емкости не должны чего-либо касаться. Ополаскивать посуду запрещается.
3.1.6. При исследовании воды из распределительных сетей отбор проб из крана производят после предварительной его стерилизации обжиганием и последующего спуска воды не менее 10 мин при полностью открытом кране. При отборе пробы напор воды может быть уменьшен. Пробу отбирают непосредственно из крана без резиновых шлангов, водораспределительных сеток и других насадок. Если через пробоотборный кран происходит постоянный излив воды, отбор проб производят без предварительного обжига, не изменяя напора воды и существующей конструкции (при наличии силиконовых или резиновых шлангов).
При заполнении емкостей должно оставаться пространство между пробкой и поверхностью воды, чтобы пробка не смачивалась при транспортировании.
После наполнения емкость закрывают стерильной пробкой и колпачком.
3.1.7. Отобранную пробу маркируют и сопровождают документом отбора проб воды с указанием места, даты, времени забора, фамилии специалиста, отбиравшего пробу, и другой информации.
3.2. Хранение и транспортирование проб
3.2.1. Доставку проб питьевой воды осуществляют в контейнерах-холодильниках при температуре (4-10) °С. В холодный период года контейнеры должны быть снабжены термоизолирующими прокладками, обеспечивающими предохранение проб от промерзания. При соблюдении указанных условий срок начала исследований от момента отбора проб не должен превышать 6 ч.
Если пробы нельзя охладить, их анализ следует провести в течение 2 ч после забора.
Если не может быть соблюдено время доставки пробы и температура хранения, анализ пробы проводить не следует.
Пробы питьевой воды должны доставляться в отдельных продезинфицированных контейнерах.
4. Оборудование, расходные материалы, реактивы, питательные среды
4.1. Оборудование
|
Термостат для температурного режима (37±1) °С |
|
|
Термостат для температурного режима (44±1) °С |
|
|
Термостат или водяная баня для температурного режима (44±0,5) °С |
|
|
Водяная баня для температурного режима (75±5) °С |
|
|
Водяная баня или термостат для температурного режима (45-49) °С (для питательных сред) |
|
|
Прибор для мембранной фильтрации под вакуумом с диаметром фильтрующей поверхности 35 или 47 мм и устройство для создания разрежения (0,5-1,0) атм. |
|
|
Весы лабораторные общего назначения 4 кл. точности, с пределом взвешивания до 1000 г |
|
|
Максимальный термометр ртутный с диапазоном измерения от 20 до 200 °С с ценой деления шкалы 1 °С |
|
|
Термометр ртутный с диапазоном измерения от 0 до 100 °С с ценой деления шкалы 0,5 °С |
|
|
рН-метр, обеспечивающий измерение с погрешностью до 0,01 |
|
|
Дистиллятор, обеспечивающий качество дистиллированной воды не ниже |
|
|
Стерилизатор суховоздушный для температурного режима (180±5) °С |
|
|
Стерилизатор паровой |
|
|
Холодильник бытовой электрический |
|
|
Вытяжной шкаф для работы с хлороформом при проведении анализа на колифаги |
|
|
Нагревательный прибор для варки питательных сред либо магнитные мешалки с подогревом до 300 °С |
|
|
Прибор для счета колоний бактерий |
|
|
Лупа с двукратным увеличением |
|
|
Дозаторы для разлива питательных сред |
|
|
Дозаторы пипеточные |
|
|
Облучатель бактерицидный |
|
|
Оптический стандарт мутности на 10 ед. |
|
|
Горелки газовые или спиртовки |
|
|
Петли бактериологические |
|
|
Поплавки бактериологические |
|
|
Пинцеты для работы с мембранными фильтрами |
|
|
Штативы для пробирок |
|
|
Емкости эмалированные |
4.2. Расходные материалы
|
Фильтрующие материалы для микробиологических целей (мембранные фильтры, аналитические трековые мембраны и другие фильтрующие материалы с диаметром пор не более 0,45 мкм и размером диска 35 или 47 мм), разрешенные к применению в установленном порядке |
|
|
Индикаторы бумажные для определения рН в диапазоне 6-8 с интервалом определения 0,2-0,3 |
|
|
Фольга алюминиевая, колпачки силиконовые, металлические |
|
|
Пипетки, вместимостью 1,5, 10 мл с ценой деления 0,1 мл многоразового или одноразового использования) |
|
|
Пробирки (многоразового или одноразового использования) |
|
|
Цилиндры, вместимостью 100, 250, 500 мл или мензурки, вместимостью 250, 500, 1000 мл |
|
|
Чашки бактериологические (Петри) |
|
|
Воронки стеклянные |
|
|
Пробки (силиконовые, резиновые и другие, выдерживающие стерилизацию сухим жаром или автоклавированием) |
|
|
Бумага фильтровальная лабораторная |
|
|
Вата хлопковая медицинская гигроскопическая |
|
|
Марля медицинская |
|
|
Карандаши или фломастеры по стеклу |
|
|
Лейкопластырь |
|
|
Перчатки резиновые |
(Измененная редакция, Изм. N 1).
4.3. Химические реактивы
Все химические реактивы должны соответствовать квалификации не ниже ч. д. а.
|
Железо серно-кислое закисное (7-водное) |
|
|
Бромтимоловый синий |
ТУ 6-09-20-86-77 |
|
Кислота соляная |
|
|
Натрий серноватисто-кислый (тиосульфат натрия) 5-водный |
|
|
Натрий хлористый |
|
|
Натрий гидрат окиси |
|
|
Калий гидрат окиси |
|
|
Спирт этиловый ректификованный медицинский |
|
|
Спирт этиловый технический |
|
|
Глюкоза |
|
|
Лактоза |
ГОСТ 6038-74 |
|
Натрий сернисто-кислый (сульфит натрия) |
ГОСТ 903-76 |
|
|
ГОСТ 5838-79 |
|
Розоловая кислота |
|
|
Фенилендиаминовые соединения* |
|
|
Фуксин основной* |
ТУ 6-09-4119-75 |
|
Хлороформ технический* |
|
|
Стрептомицин стерильный |
|
|
Йод кристаллический |
|
|
Калий йодистый |
|
|
Генциан фиолетовый кристаллический |
|
|
Фенол |
ГОСТ 6417-72 |
Примечание.
_______________
* Вещества обладают канцерогенным и мутагенным действием, работа с ними требует соблюдения мер предосторожности.
4.4. Питательные среды
|
Агар Эндо сухой |
|
|
Агар микробиологический |
|
|
Агар питательный сухой |
ТУ 42-14-33-75 |
|
Сухой препарат с индикатором ВР и лактозой или среда Гисса с лактозой |
|
|
Сухой питательный бульон |
|
|
Пептон сухой ферментативный для бактериологических целей |
|
|
Системы индикаторные бумажные (СИБ) |
- СИБ-лактоза
- СИБ-оксидаза
Допускаются к использованию коммерческие питательные среды, диагностические препараты и системы идентификации производства зарубежных фирм, предназначенные для целей описываемых методов. Питательные среды и биологические препараты зарубежного производства должны иметь международный сертификат качества ISO 9000 или EN 29 000.
При использовании следует руководствоваться рекомендациями фирмы-производителя.
Все обезвоженные коммерческие питательные среды и препараты отечественного производства должны иметь сертификат соответствия.
4.5. Тест-культуры микроорганизмов
4.5.1. Контрольный колифаг МS2, штамм ВКПМ-3254 Е. coli К12 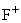
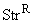 получают в ГНИИ Генетика - Всероссийской Коллекции Промышленных Микроорганизмов (ВКПМ - Россия, 113545, г.Москва, 1-ый Дорожный проезд, д.1).
получают в ГНИИ Генетика - Всероссийской Коллекции Промышленных Микроорганизмов (ВКПМ - Россия, 113545, г.Москва, 1-ый Дорожный проезд, д.1).
4.5.2. Штамм Е. coli М17-02 и один из штаммов: Pseudomonas aeruginosa или Pseudomonas fluorescens получают в Государственном Национальном Органе контроля медицинских и биологических препаратов им. Л. А. Тарасевича Минздрава России (Россия, 121002, г.Москва, ул.Сивцев-Вражек, д.41).
Примечание.
В производственных лабораториях, расположенных на территории водопроводных станций, следует использовать штамм Pseudomonas fluorescens.
5. Приготовление питательных сред и реактивов
5.1. Общие положения
Предпочтительно использование стандартизованных сухих питательных сред промышленного производства.
При использовании промышленных сухих питательных сред их приготавливают в соответствии с указаниями изготовителя на этикетке.
В этом случае следует соблюдать способ применения и срок хранения питательных сред, указанные на упаковках.
Сухие питательные среды хранят в сухих помещениях, в темноте, при комнатной температуре. Открытые упаковки тщательно закупоривают. Среды с измененным внешним видом (уплотненные, с комками), а также с истекшим сроком годности не используют.
Для приготовления растворов, реактивов и питательных сред применяют воду дистиллированную по ГОСТу 6709-72.
Питательные среды готовят в посуде из инертного материала.
Учитывая возможное изменение рН питательных сред после кипячения и стерилизации, окончательный контроль рН проводят в готовой среде при температуре 25 °С с использованием индикаторной бумаги.
После стерилизации питательные среды оставляют для охлаждения при комнатной температуре. При необходимости розлива в чашки Петри среды охлаждают до температуры (50 - 60) °С.
Температура сред, хранящихся в холодильнике, перед посевом должна быть доведена до комнатной.
5.2. Питательный бульон
5.2.1. Готовят из сухого препарата промышленного производства по способу, указанному на этикетке.
5.2.2. Питательный бульон (десятикратный) для колифагов готовят путем увеличения в 10 раз навески сухого препарата, указанной на этикетке.
5.3. Питательный агар
5.3.1. Готовят из сухого препарата промышленного производства по способу, указанному на этикетке.
5.3.2. Питательный агар для определения колифагов прямым методом готовят, увеличивая навеску сухого препарата в 2 раза от прописи.
5.3.3. Питательный агар запрещается выдерживать в расплавленном состоянии более 8 ч. Оставшийся неиспользованным агар повторному расплавлению не подлежит.
5.3.4. Полужидкий питательный агар готовят следующим образом: сухой питательный бульон (15 г) и агар микробиологический (3 г) растворить при нагревании в 1000 мл дистиллированной воды. Довести рН до 7,0-7,2, разлить в пробирки и стерилизовать автоклавированием при 121 °С в течение 15 мин.
5.3.5. Питательный агар со стрептомицином готовят из расчета содержания 100 мкг стрептомицина на 1 мл питательного агара, приготовленного по стандартной прописи. Стерильно на стерильной дистиллированной воде готовят раствор стрептомицина в концентрации 10 мг на 1 мл. В готовый питательный агар, отмеренный по объему и остуженный до температуры (45-49) °С, вносят приготовленный стерильный раствор стрептомицина из расчета 0,1 мл на 10 мл питательного агара. Разливают в пробирки для приготовления скошенного агара. Повторное расплавление питательной среды со стрептомицином запрещается.
5.4. Фуксин-сульфитная среда Эндо
5.4.1. Основная модификация
Готовят из сухого препарата по способу, указанному на этикетке. Если на поверхности среды заметны следы влаги, чашки перед посевом необходимо подсушить. Срок хранения чашек со средой не более 2-3 суток в темноте, если производителем не оговорены другие сроки.
5.4.2. Повышение дифференцирующих свойств среды
Для повышения дифференцирующих свойств среды в готовую и охлажденную до (60-70) °С среду перед разливкой в чашки допускается прибавлять на 100 мл среды 0,2 мл 5%-ного спиртового раствора основного фуксина. Срок хранения раствора фуксина - не более 1 мес.
5.4.3. Модификация среды с добавлением розоловой кислоты
В случае роста микрофлоры, не относящейся к бактериям кишечной группы, помимо фуксина, допускается добавление на 100 мл среды Эндо 0,2 мл 5%-го спиртового раствора розоловой кислоты. Срок хранения раствора розоловой кислоты - не более 1 месяца.
Модификацию среды Эндо с добавлением розоловой кислоты используют только при работе методом мембранной фильтрации.
(Измененная редакция, Изм. N 1).
5.5. Лактозо-пептонная среда
10 г пептона, 5 г натрия хлористого, 5 г лактозы растворяют при нагревании в 1 л дистиллированной воды. После растворения ингредиентов устанавливают рН 7,4-7,6, разливают по 10 мл в пробирки, стерилизуют при (112±2) °С 12 мин.
Для приготовления концентрированной лактозо-пептонной среды все ингредиенты, кроме воды, увеличивают в 10 раз, разливают по 1 мл в пробирки и по 10 мл во флаконы.
5.6. Питательные среды для подтверждения способности
ферментировать лактозу до кислоты и газа
5.6.1. Полужидкая среда с лактозой из сухого препарата
Готовят по способу, указанному на этикетке.
Срок хранения - не более 2 недель при комнатной температуре.
Посев производят уколом до дна пробирки. При образовании кислоты цвет питательной среды изменяется в соответствии с использованным индикатором. При газообразовании газ скапливается или по уколу, или на поверхности, или в толще среды появляются разрывы. При инкубации посевов более 5 ч газ может улетучиться. В таких случаях на присутствие газа указывают оставшиеся в толще среды "карманы" - потемнения среды на месте бывшего пузырька газа.
5.6.2. Полужидкая среда с лактозой
Готовят при отсутствии сухого препарата.
В 1 л дистиллированной воды растворяют 10 г пептона, 5 г натрия хлористого, (4-5) г агар-агара, доводят до кипения, устанавливают рН 7,2-7,4, добавляют 1 мл 1,6%-ного спиртового раствора бромтимолового синего. Стерилизуют при (120±2) °С 20 мин. В расплавленную среду вносят 5 г лактозы, нагревают до кипения, разливают в стерильные пробирки на высоту (3-5) см и стерилизуют при (112±2) °С 12 мин. Срок хранения - не более 2 недель при комнатной температуре.
Правильно приготовленная среда зеленого цвета с синеватым оттенком (цвет бутылочного стекла). При образовании кислоты цвет среды изменяется на желтый.
5.6.3. Лактозо-пептонная среда
Готовят по п.5.5 с добавлением 1 мл 1,6%-ного спиртового раствора бромтимолового синего на 1 л и разливают по (3-5) мл в пробирки с поплавком.
5.6.4. СИБ-лактоза
Готовят по прописи завода-изготовителя.
5.7. Реактивы для оксидазного теста
5.7.1. Вариант 1
1%-ный водный раствор тетраметил-п-фенилендиамина гидрохлорид. Готовят перед употреблением.
5.7.2. Вариант 2
Реактив N 1. 1%-ный спиртовой раствор 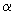 -нафтола.
-нафтола.
Реактив N 2. 1%-ный водный раствор фенилендиаминового соединения.
Растворы сохраняют в темных флаконах с притертыми пробками: 1 - до одного месяца, 2 - до одной недели. Перед употреблением к трем частям первого раствора добавляют семь частей второго раствора.
Могут быть использованы коммерческие тест-системы для постановки оксидазного теста (СИБ-оксидаза или аналоги).
Перед работой с каждой серией проб реактивы или тест-системы на оксидазу следует испытывать с тест-культурами микроорганизмов, дающих положительную (Ps. aeruginosa, Ps. fluorescens) и отрицательную оксидазную реакцию (E. coli).
5.8. Железо-сульфитный агар
В 1000 мл стерильного расплавленного питательного агара (по п.5.4) добавляют 10 г глюкозы, нагревают до растворения, разливают мерно во флаконы, автоклавируют при (112±2) °С 12 мин (основная среда).
20%-ный раствор сульфита натрия (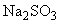 ) и 8%-ный раствор железа серно-кислого закисного (
) и 8%-ный раствор железа серно-кислого закисного (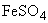 ) или железа хлористого (
) или железа хлористого (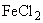 ) готовят непосредственно перед употреблением в стерильной посуде на стерильной дистиллированной воде. Раствор сульфита натрия нагревают до полного растворения. Перед выполнением анализа в 100 мл расплавленной основной среды вносят 5 мл 20%-ного раствора сульфита натрия, перемешивают, затем вносят 1 мл 8%-ного раствора сернокислого железа, перемешивают и стерильно разливают в пробирки высоким столбиком (12-15) см для работы методом мембранной фильтрации или во флаконы для работы методом прямого посева.
) готовят непосредственно перед употреблением в стерильной посуде на стерильной дистиллированной воде. Раствор сульфита натрия нагревают до полного растворения. Перед выполнением анализа в 100 мл расплавленной основной среды вносят 5 мл 20%-ного раствора сульфита натрия, перемешивают, затем вносят 1 мл 8%-ного раствора сернокислого железа, перемешивают и стерильно разливают в пробирки высоким столбиком (12-15) см для работы методом мембранной фильтрации или во флаконы для работы методом прямого посева.
5.9. Реактивы для окраски препаратов по Граму
5.9.1. Карболовый раствор генциана фиолетового готовят следующим образом: 1 г генциана фиолетового, 10 мл ректификованного этилового спирта, 5 г фенола растирают в ступке, добавляя 100 мл дистиллированной воды.
5.9.2. Раствор Люголя готовят следующим образом: 1 г йода, 2 г йодистого калия растворяют в 300 мл дистиллированной воды. Хранить во флаконе из темного стекла.
5.9.3. Фуксин Циля готовят следующим образом: 1 г основного фуксина, 10 мл спирта этилового ректификованного, 54 г фенола растирают в ступке, добавляя 100 мл дистиллированной воды.
6. Подготовка к анализу
6.1. Подготовка посуды и материалов
Лабораторную посуду моют, ополаскивают сначала водопроводной, затем дистиллированной водой и высушивают.
Пробирки, колбы, бутылки, флаконы закрывают силиконовыми или ватно-марлевыми пробками и колпачками (силиконовые, металлические, из фольги или плотной бумаги).
Пипетки со вставленными тампонами из ваты укладывают в металлические пеналы или заворачивают в бумагу.
Чашки Петри укладывают в металлические пеналы или заворачивают в бумагу. Бумага, используемая для обертывания лабораторной посуды, не должна разрушаться при стерилизации.
Подготовленную посуду стерилизуют в сушильном шкафу при температуре 160 °С в течение 2 ч или 180 °С 1 ч, считая с момента достижения указанной температуры. Стерильную посуду вынимают из стерилизационного шкафа после его охлаждения ниже 60 °С. Срок хранения стерильной посуды - не более 10 дней.
Материалы и лабораторную посуду, разрушающиеся при температуре (160-180) °С (резина и т.п.), следует стерилизовать в паровом стерилизаторе при температуре (121±2) °С 20 мин.
Новые резиновые пробки кипятят в 2%-ном растворе натрия двууглекислого 30 мин и 5 раз промывают водопроводной водой (кипячение и промывание повторяют дважды). Затем пробки кипятят в дистиллированной воде 30 мин, высушивают, заворачивают в бумагу или фольгу и стерилизуют в паровом стерилизаторе. Резиновые пробки, использованные ранее, обеззараживают, кипятят 30 мин в водопроводной воде с нейтральным моющим средством, промывают в водопроводной воде, высушивают, монтируют и стерилизуют.
После выполнения анализа все использованные чашки, пробирки и пипетки обеззараживают в автоклаве при (126±2) °С в течение 60 мин, в исключительных случаях допускается обеззараживание кипячением в 2%-ном растворе пищевой соды или 0,5%-ном моющего средства в течение 60 мин с момента закипания (в закрытой емкости с полным погружением в раствор).
6.2. Подготовка проб воды
Перед посевом пробу тщательно перемешивают и фламбируют горящим тампоном край емкости. Используемые пробирки и чашки маркируют.
Перед каждым отбором новой порции воды для анализа пробу перемешивают стерильной пипеткой.
7. Методика работы при использовании фильтрующих материалов
7.1. Подготовка фильтрующих материалов
Фильтрующие материалы должны быть подготовлены к анализу в соответствии с указаниями изготовителя.
7.2. Подготовка фильтровального аппарата
Воронку и столик фильтровального аппарата обтирают марлевым (ватным) тампоном, смоченным спиртом ректификованным, и фламбируют. После охлаждения на столик фильтровального аппарата кладут фламбированным пинцетом стерильный фильтрующий материал, прижимают его воронкой.
7, 7.1, 7.2 (Измененная редакция, Изм. N 1).
7.3. Фильтрование воды
В воронку прибора для фильтрования наливают отмеренный объем воды, затем создают вакуум.
При посеве нескольких объемов одной пробы следует фильтровать через один фильтровальный аппарат без обеззараживания сначала меньшие, а затем большие объемы воды, меняя каждый раз фильтры. Перед фильтрованием каждой новой пробы прибор обеззараживают.
Следует начинать с фильтрования проб обеззараженной воды или тех проб, которые предположительно не загрязнены, а затем фильтровать загрязненные пробы.
При фильтровании 1 мл исследуемой воды следует в воронку налить предварительно не менее 10 мл стерильной воды, а затем внести анализируемую воду.
После окончания фильтрования и осушения фильтра отключают вакуум, воронку снимают, фильтр осторожно поднимают за край фламбированным пинцетом и переносят его, не переворачивая, на питательную среду, разлитую в чашки Петри, избегая пузырьков воздуха между средой и фильтром. Поверхность фильтра с осевшими на ней бактериями должна быть обращена вверх.
Под каждым фильтром на дне чашки делают надпись с указанием объема профильтрованной воды, номера пробы и даты посева. На одну чашку можно поместить 3-4 фильтра с условием, чтобы фильтры не соприкасались.
8. Проведение анализа
8.1. Определение общего числа микроорганизмов, образующих колонии на питательном агаре
8.1.1. Определение понятия показателя
Метод определяет в питьевой воде общее число мезофильных аэробных и факультативно анаэробных микроорганизмов (ОМЧ), способных образовывать колонии на питательном агаре при температуре 37 °С в течение 24 ч, видимые с увеличением в 2 раза.
8.1.2. Выполнение анализа
Из каждой пробы делают посев не менее двух объемов по 1 мл.
После тщательного перемешивания пробы воды вносят по 1 мл в стерильные чашки Петри, слегка приоткрывая крышки. После внесения воды в каждую чашку вливают (8-12) мл (на чашку диаметром 90-100 мм) расплавленного и остуженного до (45-49) °С питательного агара после фламбирования края посуды, в которой он содержится. Затем быстро смешивают содержимое чашек, равномерно распределяя по всему дну, избегая образования пузырьков воздуха, попадания агара на края и крышку чашки. Эту процедуру производят на горизонтальной поверхности, где чашки оставляют до застывания агара.
Расплавленный агар на период проведения анализа помещают в водяную баню или термостат, поддерживающие температуру (45-49) °С.
После застывания агара чашки с посевами помещают в термостат вверх дном и инкубируют при температуре (37±1) °С в течение (24±2) ч.
8.1.3. Учет результатов
Подсчитывают все выросшие на чашке колонии, наблюдаемые при увеличении в 2 раза. Учитывают только те чашки, на которых выросло не более 300 изолированных колоний.
Количество колоний на обеих чашках суммируют и делят на два. Результат выражают числом колониеобразующих единиц (КОЕ) в 1 мл исследуемой пробы воды.
Если на одной из 2 чашек подсчет невозможен, результат выдают на основании учета колоний на одной чашке. Если на двух чашках имеет место рост расплывчатых колоний, не распространяющийся на всю поверхность чашки, или выросло более 300 колоний и анализ нельзя повторить, подсчитывают сектор чашки с последующим пересчетом на всю поверхность. В этих случаях в протоколе отмечают "число КОЕ/мл - ориентировочно".
Если подсчет колоний на чашках невозможен, то в протоколе отмечают "сплошной рост".
8.2. Определение общих и термотолерантных колиформных бактерий
методом мембранной фильтрации (основной метод)
8.2.1. Определение понятия показателя
Общие колиформные бактерии (ОКБ) - грамотрицательные, оксидазоотрицательные, не образующие спор палочки, способные расти на дифференциальных лактозных средах, ферментирующие лактозу до кислоты, альдегида и газа при температуре (37+1) °С в течение (24-48) ч.
Термотолерантные колиформные бактерии (ТКБ) входят в число общих колиформных бактерий, обладают всеми их признаками и, кроме того, способны ферментировать лактозу до кислоты, альдегида и газа при температуре (44±0,5) °С в течение 24 ч.
8.2.2. Принцип метода
Метод основан на фильтрации установленного объема воды через фильтрующие материалы, выращивании посевов на дифференциальной питательной среде с лактозой и последующей идентификации колоний по культуральным и биохимическим свойствам.
(Измененная редакция, Изм. N 1).
8.2.3. Выполнение анализа
8.2.3.1. Порядок исследования
При исследовании питьевой воды анализируют 3 объема по 100 мл.
При получении стабильных отрицательных результатов допустима фильтрация 300 мл воды через один фильтр.
При фильтрации воды неизвестного качества целесообразно увеличение количества фильтруемых объемов для получения изолированных колоний на фильтре (например, 10, 40, 100, 150 мл воды).
Отмеренный объем воды фильтруют с соблюдением требований, изложенных в п.7.
Фильтры помещают на среду Эндо, приготовленную по п.5.4. Чашки с фильтрами ставят в термостат дном вверх и инкубируют посевы при температуре (37±1) °С в течение (24±2) ч.
Если на фильтрах нет роста или выросли колонии пленчатые, губчатые, плесневые, прозрачные, расплывчатые, выдают отрицательный ответ: отсутствие ОКБ и ТКБ в 100 мл исследуемой воды. Анализ заканчивают через 24 ч.
Если на фильтрах обнаружен рост изолированных типичных лактозоположительных колоний: темно-красных, красных с металлическим блеском или без него или других подобного типа колоний с отпечатком на обратной стороне фильтра, подсчитывают число колоний каждого типа отдельно и приступают к подтверждению их принадлежности к ОКБ и ТКБ.
Для подтверждения наличия ОКБ исследуют:
- все колонии, если на фильтрах выросло менее 5 колоний;
- не менее 3 - 4 колоний каждого типа.
Для подтверждения наличия ТКБ исследуют все типичные колонии, но не более 10.
Каждую выбранную изолированную колонию исследуют на:
- наличие оксидазной активности;
- принадлежность к Граму (микроскопия окрашенного по Граму препарата или постановка теста Грегерсена);
- ферментацию лактозы до кислоты и газа.
(Измененная редакция, Изм. N 1).
8.2.3 2. Постановка оксидазного теста
Полоску фильтровальной бумаги помещают в чистую чашку Петри и смачивают 2-3 каплями реактива для оксидазного теста по п.5.7. Готовые бумажные системы смачивают дистиллированной водой. Часть изолированной колонии стеклянной палочкой или платиновой петлей (металлическая петля из нихрома может дать ложноположительную реакцию) наносят штрихом на подготовленную фильтровальную бумагу. Реакция считается положительной, если в течение 1 мин появляется фиолетово-коричневое (п.5.7.1 вариант 1) или синее (п.5.7.2 вариант 2 и СИБ-оксидаза) окрашивание штриха. При отрицательной реакции цвет в месте нанесения культуры не меняется. При положительном результате эту колонию из дальнейшего исследования исключают.
Если при исследовании колоний, окрашенных в темно-красный цвет, получают недостаточно четкий результат, необходимо пересеять культуру со среды Эндо на питательный агар. После инкубации тест повторяют.
8.2.3.3. Определение принадлежности к Граму
Из оксидазоотрицательной колонии делается мазок, окрашивается по Граму и микроскопируется.
На обезжиренное спиртом предметное стекло наносят петлей 1 каплю дистиллированной воды, вносят небольшое количество культуры из анализируемой колонии и распределяют по поверхности стекла. Мазок высушивают при комнатной температуре и фиксируют трехкратным проведением через пламя горелки. На препарат накладывают полоску фильтровальной бумаги и на нее наливают карболовый раствор генциана фиолетового на (0,5-1) мин, снимают бумагу, наливают раствор Люголя на (0,5-1) мин, сливают раствор Люголя и стекло промывают в этиловом спирте в течение (0,5-1) мин, пока не перестанет отходить краситель. Затем стекло тщательно промывают водой и докрашивают в течение (1-2) мин фуксином Циля, разведенным 1:10 дистиллированной водой. После промывания и просушивания препарата мазок микроскопируют.
Приготовление реактивов для окраски по Граму изложено в п.5.9.
Грамотрицательные микроорганизмы имеют розовую окраску, грамположительные окрашиваются в синий цвет. Колиформные бактерии являются грамотрицательными палочками.
Окраска по Граму может быть заменена тестом Грегерсена, не требующим использования оптики.
Тест Грегерсена: в капле 3%-ного водного раствора КОН на предметном стекле эмульгируют бактерийную массу, взятую с плотной среды. После нескольких секунд перемешивания петлей взвесь ослизняется и за петлей тянутся слизистые нити, что указывает на принадлежность испытуемой культуры или колонии к грамотрицательному виду. У грамположительных бактерий слизистые нити не образуются - реакция отрицательная.
8.2.3.4. Определение ферментации лактозы
Оставшуюся часть оксидазоотрицательной грамотрицательной изолированной колонии засевают параллельно в две пробирки с лактозной средой (п.5.6):
- для подтверждения наличия ОКБ посев инкубируют при температуре (37±1) °С в течение 48 ч;
- для подтверждения наличия ТКБ посев осуществляют в среду, предварительно прогретую до температуры (43-44) °С, и инкубируют при температуре (44±0,5) °С в течение 24 ч.
Первичный учет образования кислоты и газа на подтверждающих полужидких средах и СИБ (п.5.6) возможен через (4-6) ч. При обнаружении кислоты и газа дают положительный ответ. При отсутствии кислоты и газа или при наличии только кислоты пробирки с посевами для окончательного учета ТКБ оставляют до 24 ч. Пробирки с посевами для подтверждения наличия ОКБ после просмотра через 24 ч и получения отрицательного результата оставляют для окончательного учета до 48 ч.
Если колония, подлежащая исследованию, незначительных размеров, ее пересевают на скошенный питательный агар и после инкубации в течение (18-24) ч выполняют все необходимые подтверждающие тесты.
8.2.3.5. Постановка подтверждающих тестов при наложении колоний или сплошном росте
Если на части или на всей поверхности фильтра наблюдается наложение колоний или сплошной рост, выполняют оксидазный тест. Фильтрующий материал помещают на кружок фильтровальной бумаги большего диаметра, чем фильтр, обильно смоченный реактивом, или на диск СИБ-оксидаза, смоченный дистиллированной водой. При появлении первых признаков реакции, но не более чем через 5 мин, фильтрующий материал переносят обратно на среду Эндо. После четкого проявления реакции определяют результат. При появлении фиолетово-коричневого или синего окрашивания (в зависимости от примененного реактива) оксидазный тест считают положительным.
Если на фильтрах все колонии оксидазоположительные, они не учитываются и выдают ответ об отсутствии ОКБ и ТКБ и завершают анализ.
При отрицательной оксидазной реакции проводят рассев до получения изолированных колоний и подтверждают их принадлежность к ОКБ и ТКБ по п.п.8.2.3.3-8.2.3.4 (анализ качественный).
(Измененная редакция, Изм. N 1).
8.2.4. Учет результатов
8.2.4.1. Грамотрицательные колонии учитываются как ОКБ при отрицательном оксидазном тесте и ферментации лактозы при температуре 37 °С с образованием кислоты и газа.
Грамотрицательные колонии учитываются как ТКБ при отрицательном оксидазном тесте и ферментации лактозы при температуре 44 °С с образованием кислоты и газа.
8.2.4.2. При отсутствии общих и термотолерантных колиформных бактерий на всех фильтрах результат записывают "не обнаружено КОЕ ОКБ в 100 мл" и "не обнаружено КОЕ ТКБ в 100 мл".
8.2.4.3. В случае идентификации всех выросших подозрительных колоний число колониеобразующих единиц ОКБ и ТКБ подсчитывают на всех фильтрах и выражают результат анализа КОЕ в 100 мл воды.
Вычисление проводят по формуле:
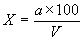 , где
, где
 - число колоний в 100 мл;
- число колоний в 100 мл;
 - профильтрованный объем воды через фильтры, на которых велся учет;
- профильтрованный объем воды через фильтры, на которых велся учет;
 - число подсчитанных на этих фильтрах колоний в сумме.
- число подсчитанных на этих фильтрах колоний в сумме.
Примеры:
-
1. При посеве 3 фильтров по 100 мл выросло две колонии в 100 мл, на остальных двух фильтрах нет роста. Число общих или термотолерантных колиформных бактерий будет:
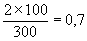 КОЕ ОКБ (ТКБ) в 100 мл
КОЕ ОКБ (ТКБ) в 100 мл -
2. При посеве 10, 40, 100 и 150 мл на фильтрах с профильтрованным объемом 40 мл выросло 4 изолированные колонии, с профильтрованным объемом 100 - 3 ОКБ. Фильтры с объемами 10 мл и 150 мл заросли и учету не подлежат. Суммируют общее число колоний ОКБ (ТКБ) на тех фильтрах, где получены изолированные колонии, и пересчитывают на объем 100 мл.
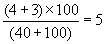 КОЕ в 100 мл
КОЕ в 100 мл
8.2.4.4. Если при выборочной проверке колоний одного типа получены неодинаковые результаты, то вычисляют числа ОКБ или ТКБ среди колоний этого типа по формуле:
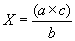 , где
, где
 - число подтвержденных бактерий одного типа;
- число подтвержденных бактерий одного типа;
 - общее число колоний этого типа;
- общее число колоний этого типа;
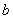 - число проверенных из них;
- число проверенных из них;
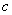 - число колоний с положительным результатом.
- число колоний с положительным результатом.
Полученные результаты учета по каждому типу колоний суммируют и далее подсчитывают по п.8.2.4.3-8.2.4.4.
8.2.4.5. Окончательный результат выдают: количество КОЕ ОКБ в 100 мл, из них количество КОЕ ТКБ в 100 мл.
Ориентировочный результат может быть выдан при обнаружении типичных колиформных колоний на среде Эндо, образованных грамотрицательными оксидазоотрицательными бактериями. Окончательный ответ подтверждается по результатам ферментации лактозы.
8.2.4.6. При наложении колоний или сплошном росте на всех фильтрах (п.8.2.3.5) в случае подтверждения принадлежности к ОКБ и ТКБ выдается качественный результат "обнаружено ОКБ в 100 мл".
Если все колонии на фильтре оксидазоположительные или не подтвердилась их принадлежность к ОКБ и ТКБ, анализ завершается, в протоколе отмечают "зарост фильтров".
В обоих случаях анализ повторяют.
8.3. Определение общих и термотолерантных колиформных бактерий титрационным методом
8.3.1. Определение понятия показателя
Определение понятия показателей ОКБ и ТКБ по п.8.2.1.
8.3.2. Область применения
Титрационный метод может быть использован:
- при отсутствии материалов и оборудования, необходимых для выполнения анализа методом мембранной фильтрации;
- при анализе воды с большим содержанием взвешенных веществ;
- в случае преобладания в воде посторонней микрофлоры, препятствующей получению на фильтрах изолированных колоний общих колиформных бактерий.
8.3.3. Принцип метода
Метод основан на накоплении бактерий после посева установленного объема воды в жидкую питательную среду, с последующим пересевом на дифференциальную плотную питательную среду с лактозой и идентификации колоний по культуральным и биохимическим тестам.
8.3.4. Выполнение анализа
При исследовании питьевой воды качественным методом (текущий санэпиднадзор, производственный контроль) засевают 3 объема по 100 мл.
При исследованиях воды с целью количественного определения ОКБ и ТКБ при повторном анализе производят посев: 3 объемов по 100 мл, 3 объемов по 10 мл, 3 объемов по 1 мл.
Каждый объем исследуемой воды засевают в лактозо-пептонную среду, приготовленную по п.5.5. Посев 100 мл и 10 мл воды производят в 10 и 1 мл концентрированной лактозо-пептонной среды, посев 1 мл пробы проводят в 10 мл среды обычной концентрации.
Посевы инкубируют при (37±1) °С в течение 48 ч. Не ранее 24 час инкубации проводят предварительную оценку посевов. Из емкостей, где отмечено наличие роста (помутнение) и образование газа, производят высев бактериологической петлей на сектора среды Эндо (п.5.4.1) для получения изолированных колоний.
Емкости без наличия роста и образования газа оставляют в термостате и окончательно просматривают через 48 ч. Посевы без признаков роста считают отрицательными и дальнейшему исследованию они не подлежат. Из емкостей, где отмечено помутнение и образование газа или только помутнение, делают высев на сектора среды Эндо.
Посевы на среде Эндо инкубируют при температуре (37±1) °С в течение (18-20) ч.
При образовании помутнения и газа в среде накопления и росте на среде Эндо колоний, типичных для лактозоположительных бактерий: темно-красных или красных, с металлическим блеском или без него, выпуклых с красным центром и отпечатком на питательной среде, дают положительный ответ на присутствие общих колиформных бактерий в данном объеме пробы.
Наличие ОКБ требуется подтвердить:
- если в среде накопления отмечено только помутнение;
- если принадлежность к лактозоположительным колониям вызывает сомнение у исследователя.
В этих случаях:
- проверяют наличие отпечатка на среде Эндо после снятия петлей подозрительной колонии;
- выполняют оксидазный тест по п.8.2.3.2;
- подтверждают принадлежность к Граму по п.8.2.3.3;
- подтверждают способность к газообразованию при посеве изолированных 1-2 колоний каждого типа с каждого сектора на среду с лактозой по п.5.6 с последующей инкубацией посевов при температуре (37±1) °С в течение (24-48) ч.
При отсутствии изолированных колоний проводят рассев на среду Эндо общепринятыми бактериологическими методами.
Отрицательный ответ дают, если:
- в среде накопления нет признаков роста;
- на секторах среды Эндо нет роста;
- на секторах среды Эндо выросли не характерные для колиформных бактерий колонии (прозрачные с неровными краями, расплывчатые и т.п.);
- все колонии оказались оксидазоположительными;
- все колонии оказались грамположительными;
- если в подтверждающем тесте на среде с углеводом не отмечено газообразования.
Для определения термотолерантных колиформных бактерий работают с секторами среды Эндо, где выросли типичные лактозоположительные колонии. Делают посев 2-3 изолированных колоний каждого типа с каждого сектора в пробирки с любой из лактозных сред, приготовленных по п.5.6.
Среду перед посевом нагревают на водяной бане или в термостате до 44 °С. Немедленно после посева пробирки помещают в термостат и инкубируют при температуре (44±0,5) °С в течение 24 ч. Допускается просмотр посевов через (4-6) ч.
При образовании газа в среде накопления, росте на среде Эндо лактозоположительных бактерий и выявлении способности этих бактерий ферментировать лактозу до кислоты и газа в течение 24 ч при температуре 44 °С дают положительный ответ на наличие в этом объеме пробы воды ТКБ. Во всех остальных случаях дают отрицательный ответ.
Допустимо для ускорения выдачи ответа на присутствие ТКБ производить высев 1 мл из объемов среды накопления, где отмечено помутнение и газообразование в пробирке с лактозо-пептонной средой с поплавком по п.5.6 и прогретой предварительно до температуры 44 °С. Посевы выдерживают в термостате при температуре (44±0,5) °С в течение 24 ч. При обнаружении кислоты и газа дают положительный ответ.
8.3.5. Учет результатов
При исследовании 3 объемов по 100 мл результаты оцениваются качественно и при обнаружении ОКБ и ТКБ хотя бы в одном из 3 объемов, делается запись в протоколе "обнаружены в 100 мл".
При исследовании количественным методом определяют наиболее вероятное число (НВЧ) ОКБ и ТКБ по табл.1.1 приложения 1.
Результат сообщают без доверительного интервала.
При отрицательном ответе на наличие ОКБ и ТКБ во всех исследованных объемах выдают заключение в протоколе "не обнаружены в 100 мл".
8.4. Определение спор сульфитредуцирующих клостридий
8.4.1. Определение понятия показателя
Сулъфитредуцирующие клостридии - спорообразующие анаэробные палочковидные микроорганизмы, редуцирующие сульфит натрия на железо-сульфитном агаре при температуре (44±1) °С в течение (16-18) ч.
8.4.2. Принцип метода
Метод основан на выращивании посевов в железо-сульфитном агаре в условиях, приближенных к анаэробным, и подсчете числа черных колоний.
8.4.3. Выполнение анализа
8.4.3.1. Пробу воды 20 мл прогревают на водяной бане в пробирках при температуре (75±5) °С в течение 15 мин для исключения вегетативных форм.
При исследовании хлорированной воды прогревание пробы можно не производить.
Из каждой пробы питьевой воды делают посев или фильтруют 20 мл. При необходимости подбирают объемы с таким расчетом, чтобы в посевах (на фильтрах) выросло не более 10-15 колоний. При этом ориентируются на результаты предыдущих исследований.
Фильтрование воды производят в соответствии с требованиями, изложенными в п.7.
8.4.3.2. Определение методом фильтрования в пробирках
Перед посевом пробирки с железо-сульфитным агаром, приготовленным по п.5.8, расплавляют на водяной бане (не кипятить!). В течение посева поддерживают среду нагретой до (70-80) °С в водяной бане.
После фильтрования установленного объема воды фильтрующий материал фламбированным пинцетом берут за два противоположных края и согнутый в виде трубочки помещают в пробирку с горячим агаром. Сторона фильтра с осевшими бактериями обращена внутрь. При этом фильтр распрямляется и располагается по стенке пробирки.
Сразу же после посева пробирку с агаром и фильтром для создания анаэробных условий быстро охлаждают, помещая в емкость с холодной водой. Культивируют посевы при (44±1) °С в течение (16-18) ч.
(Измененная редакция, Изм. N 1).
8.4.3.3. Определение методом фильтрования в чашках Петри
Чашки Петри диаметром (55-60) мм заливают тонким слоем железо-сульфитного агара. После фильтрации фильтр поместить фильтрующей поверхностью вниз на застывшую питательную среду так, чтобы под фильтром не было пузырьков воздуха. Затем заливают расплавленным железо-сульфитным агаром до верхнего края чашки, чтобы крышка плотно прилегала к среде для создания анаэробных условий. Культивируют посевы при (44±1) °С в течение (16-18) ч.
8.4.3.4. Определение прямым посевом
Железо-сульфитный агар во флаконах и пробу воды готовят, как это описано в п.8.4.3.1.
В стерильные пробирки вносят:
- по 10 мл в 2 пробирки (объемом не менее 30 мл) или
- по 5 мл в 4 пробирки (объемом по 15 мл).
Посевы заливают горячим железо-сульфитным агаром в количестве, превышающем объем воды в 2 раза. Среду заливать по стенке пробирки, избегая образования пузырьков воздуха. После этого пробирку быстро охлаждают, помещая ее в емкость с холодной водой для создания анаэробных условий. Посевы инкубируют при (44±1) °С в течение (16-18) ч.
8.4.4. Учет результатов
Количественному учету подлежат только те посевы, где получены изолированные колонии. Подсчитывают черные колонии, выросшие как на фильтрах, так и в толще питательной среды.
Результат анализа выражают числом колониеобразующих единиц (КОЕ) спор сульфитредуцирующих клостридий в 20 мл воды.
При отсутствии роста черных колоний на всех фильтрах дают ответ "не обнаружено в 20 мл воды".
При невозможности учета колоний из-за сливного роста результат оценивается как качественный, в протоколе отмечают "обнаружено в 20 мл". При необходимости получения количественного результата анализ повторяют.
8.5. Определение колифагов
8.5.1. Определение понятия показателя
Колифаги - бактериальные вирусы, способные лизировать E. coli и формировать при температуре (37±1) °С через (18±2) ч зоны лизиса бактериального газона (бляшки) на питательном агаре.
8.5.2. Титрационный метод определения колифагов
8.5.2.1. Принцип метода
Определение колифагов в питьевой воде заключается в предварительном накоплении колифагов в среде обогащения на культуре E. coli и последующем выявлении зон лизиса (просветления) газона E. coli на питательном агаре.
8.5.2.2. Область применения
Метод предназначен для проведения текущего контроля качества питьевой воды.
8.5.2.3. Подготовка тест-культуры E. coli К12 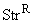 .
.
На всех этапах исследования используют бактериальную взвесь, приготовленную следующим образом: культуру E. coli засевают в пробирку со скошенным питательным агаром со стрептомицином (п.5.3.5). Через (18±2) ч инкубации при температуре (37±1) °С произвести смыв бактерий с косяка 5 мл стерильного физиологического раствора (0,85%-ный раствор 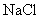 ) и по стандарту мутности готовят взвесь E. coli в концентрации 10
) и по стандарту мутности готовят взвесь E. coli в концентрации 10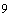 бактериальных клеток в 1 мл.
бактериальных клеток в 1 мл.
Допускается использование 4-часовой бульонной культуры E. coli, полученной путем подращивания в термостате при температуре 37 °С. Концентрация 10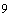 бактериальных клеток E. coli содержится в 2 мл.
бактериальных клеток E. coli содержится в 2 мл.
8.5.2.4. Проведение качественного анализа
В исследуемую пробу воды объемом 100 мл вносят 10 мл 10-кратного питательного бульона (приготовленного по п.5.2.2) и 1 мл подготовленного смыва тест-культуры или 2 мл 4-часовой бульонной культуры (п.8.5.2.3).
Для контроля культуры 0,1 мл смыва бактерий Е. coli (или 0,2 мл 4-часовой бульонной культуры) помещают в чашку Петри и заливают питательным агаром.
Исследуемую пробу воды (100 мл) и чашку Петри с контролем E. coli помещают в термостат и инкубируют при температуре (37±1) °С в течение (18±2) ч.
После инкубации из исследуемой пробы воды отливают в пробирку 10 мл и добавляют 1 мл хлороформа.
Пробирку закрывают стерильной резиновой или силиконовой пробкой, энергично встряхивают для равномерного распределения хлороформа по объему пробы и оставляют при комнатной температуре не менее 15 мин до полного осаждения хлороформа.
В предварительно расплавленный и остуженный до (45-49) °С питательный агар добавляют приготовленный смыв бактерий E. coli (п.8.5.2.3) из расчета 1,0 мл смыва (или 2 мл 4-часовой бульонной культуры) на 100 мл агара.
В стерильную чашку Петри пипеткой из пробирки переносят 1 мл обработанной хлороформом пробы (не касаясь хлороформа) и заливают смесью расплавленного и остуженного до (45-49) °С питательного агара объемом (12-15) мл, а также одну дополнительную чашку Петри для контроля культуры E. coli и осторожно покачивают для равномерного перемешивания пробы воды и агара. Для полного застывания чашки оставляют на столе при комнатной температуре на 10 мин. После застывания чашки переворачивают и помещают в термостат на (18±2) ч при 37 °С.
При выполнении серии проб ставится общий контроль для всей серии.
Учет результатов
Просмотр посевов осуществляют в проходящем свете.
Проба считается положительной при наличии полного лизиса, просветления нескольких бляшек, одной бляшки на чашке с пробой воды при отсутствии зон лизиса на контрольной чашке.
В протоколе анализа отмечается: колифаги обнаружены или не обнаружены в 100 мл воды (результат качественный).
При наличии зон лизиса в контроле культуры результат считается недействительным.
8.5.2.5. Проведение количественного анализа
Исследуемую пробу воды в количестве 100 мл разлить на 6 объемов: 1 флакон 50 мл и 5 пробирок по 10 мл. В 50 мл пробы добавить 5 мл десятикратного питательного бульона (по п.5.2.2) и 0,5 мл смыва (или 1 мл 4-часовой бульонной культуры) бактерий E. coli (п.8.5.2.3). В каждые 10 мл пробы внести по 1 мл десятикратного питательного бульона и 0,1 мл смыва (или 0,2 мл 4-часовой бульонной культуры) бактерий E. coli.
Для контроля культуры 0,1 мл смыва бактерий (или 0,2 мл 4-часовой бульонной культуры) E. coli помещают в чашку Петри и заливают питательным агаром.
Посевы инкубируют при температуре (37±1) °С в течение 18±2 ч.
После инкубации из объема 50 мл отлить в пробирку 10 мл. Во все исследуемые 6 объемов добавить по 1 мл хлороформа. Пробирки закрыть стерильными резиновыми или силиконовыми пробками, энергично встряхнуть для равномерного распределения хлороформа по объему пробы и оставить при комнатной температуре не менее 15 мин для осаждения хлороформа.
В предварительно расплавленный и остуженный до (45-49) °С питательный агар добавить приготовленный смыв бактерий E. coli (п.8.5.2.3) из расчета 1,0 мл смыва (или 2 мл 4-часовой бульонной культуры) на 100 мл агара. Приготовленную смесь разлить в чашки Петри: 1 чашку для контроля культуры E. coli на лизогенность и по одной чашке на каждую исследуемую пробу воды. При одновременном анализе нескольких проб воды ставится один контроль культуры E. coli.
После застывания агара чашки, предназначенные для посева проб, разделить на 6 секторов, промаркировать их в соответствии с исследуемыми объемами. На каждый сектор из соответствующей пробирки нанести пастеровской пипеткой (микропипеткой или бактериологической петлей продольным штрихом) по 1 капле надосадочной жидкости (без хлороформа).
После подсыхания капель чашки с исследуемыми пробами и контрольную чашку поместить в термостат при (37±1) °С на (18±2) ч.
Учет результатов
Просмотр результатов осуществляется в проходящем свете.
Учет проводится по наличию зон просветления (лизиса) на секторах газона E. coli.
При применении капельного способа посева пипеткой образуется зона лизиса в виде округлого пятна или отдельных бляшек. При посеве продольным штрихом бактериологической петлей отмечается лизис по ходу штриха.
Проба считается положительной при наличии зоны лизиса хотя бы на одном секторе при отсутствии зон лизиса на контрольной чашке.
Оценка проводится по таблице наиболее вероятного числа (НВЧ) бляшкообразующих единиц (БОЕ) (табл.1.2). В протоколе анализа указывается наиболее вероятное количество колифагов в 100 мл воды и диапазон возможных колебаний: НВЧ БОЕ (нижний предел - верхний предел) колифагов в 100 мл. Результат полуколичественный.
При наличии зон лизиса в контрольной чашке результат считать недействительным.
8.5.3. Прямой метод определения колифагов
8.5.3.1. Принцип метода
Определение колифагов в питьевой воде заключается в исследовании нормируемого объема воды (100 мл) путем его прямого посева и последующего учета зон лизиса (бляшек) на газоне E. coli в чашках Петри с питательным агаром.
8.5.3.2. Область определения
Прямой метод выделения колифагов из воды проводят параллельно с титрационным при исследованиях по эпидемическим показаниям.
8.5.3 3. Проведение анализа
В питательный агар двойной концентрации (п.5.3.2), расплавленный и остуженный до (45-49) °С, добавить смыв E. coli (п.8.5.2.3) из расчета 2,0 мл смыва (или 4 мл 4-часовой бульонной культуры) на каждые 100 мл агара, перемешать. Исследуемые 100 мл воды разлить по 20 мл в большие пробирки, нагреть до (35-44) °С и немедленно (не более чем через 5 мин по достижении требуемой температуры) разлить в 5 чашек Петри и сразу же внести в каждую чашку по 20 мл смеси агара с культурой E. coli.
Для контроля культуры E. coli в одну чашку Петри внести 20 мл стерильной водопроводной воды, предварительно прогретой до (35-44) °С, залить 20 мл приготовленного агара с E. coli и осторожно перемешать.
Содержимое чашек осторожно перемешать и оставить при комнатной температуре до застывания. Чашки с застывшим агаром поместить дном вверх в термостат и инкубировать при температуре (37±1) °С в течение (18±2) ч.
Учет результатов
Просмотр посевов осуществляется в проходящем свете.
Учет результатов проводят путем подсчета и суммирования бляшек, выросших на 5 чашках Петри. Результаты выражают в бляшкообразующих единицах (БОЕ) на 100 мл пробы воды. В контрольной чашке бляшки должны отсутствовать.
Наиболее часто зоны лизиса выглядят прозрачными пятнами на фоне газона тест-культуры питательного агара в виде круглых изолированных бляшек (от 1 до 5-7) мм в диаметре с четко выраженными либо стертыми границами.
При высоких концентрациях фага наблюдается разная картина лизиса.
Слияние негативных колоний дает "ажурный" газон E. coli, рост единичных колоний E. coli на фоне сплошного лизиса, либо полное отсутствие роста на чашке.
При прямом посеве возможен лизис, маскируемый негомогенно застывшим агаром, а также закрытый сопутствующей микрофлорой. Капли конденсата и негомогенно застывший при прямом посеве агар могут приводить к образованию артефактов на газоне E. coli, визуально напоминающих лизис.
Предварительный учет результатов можно проводить через (5-6) ч инкубации. На этом этапе при наличии четких зон лизиса может быть выдан предварительный ответ о присутствии колифагов в воде.
Окончательный количественный учет прямого посева проводится через (18±2) ч. Результаты выражают количеством бляшкообразующих единиц (БОЕ) на 100 мл пробы воды.
Если отмечен сливной рост бляшек и счет затруднителен, то по данным прямого посева может быть выдан качественный результат: "обнаружено в 100 мл воды".
При получении отрицательного результата при работе прямым методом окончательный ответ выдается по результатам титрационного метода.
При наличии зон лизиса в контрольной чашке результат исследования считается недействительным.
8.5.4. Постановка контролей
8.5.4.1. Отрицательный контроль
Отрицательный контроль подтверждает отсутствие контаминации фагом питательных сред, лабораторной посуды, оборудования на этапах подготовки и проведения анализа, а также позволяет оценить способность тест-культуры E. coli давать равномерный газон.
Отрицательным контролем служит исследование стерильной водопроводной воды, проводимое аналогично анализируемой пробе воды. Так, при анализе воды титрационным методом 10 мл стерильной водопроводной воды вносят в дополнительную пробирку. При анализе воды прямым посевом в дополнительную шестую чашку Петри вносят 20 мл стерильной водопроводной воды.
Дополнительные посевы исследуются на колифаги аналогично основным пробам.
При анализе серии проб отрицательный контроль может быть один на каждый вид анализа: титрационный и прямой. В этом случае постановка отрицательного контроля поэтапно осуществляется после обработки всех проб данной серии.
В случае обнаружения бляшек колифагов в чашках с отрицательным контролем результаты исследования всей серии проб воды недействительны.
Следует проверить стерильность лабораторного оборудования, посуды, питательных сред, а также повторить контрольный посев на чистоту тест-штамма E. coli К12 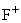
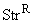 .
.
Кратность проведения отрицательного контроля - 1 раз в день.
8.5.4.2. Методика подтверждения фаговой природы лизиса
В сомнительных случаях при работе как титрационным, так и прямым методами необходимо провести контрольный посев на подтверждение фаговой природы лизиса.
С этой целью бактериологической петлей извлекают участок агара, подозрительный на колифаги, помещают его в 5 мл питательного бульона, куда добавляют каплю тест-культуры E. coli и инкубируют при 37 °С в течение (16-18) ч. Полученную культуру обрабатывают хлороформом и исследуют на наличие фага. Высев осуществляют петлей или пипеткой на сектора питательного агара аналогично способу, описанному в п.8.5.2.5. Лизис на любом из секторов расценивается как подтверждение наличия фага.
Приложения
Приложение 1
Таблицы расчета наиболее вероятного числа микроорганизмов
Таблица 1.1
Расчет наиболее вероятного числа бактерий в 100 мл питьевой воды
|
Число положительных результатов из: |
НВЧ бактерий в 100 мл |
Доверительный интервал (95%) |
|||
|
3 объемов по 100 мл |
3 объемов по 10 мл |
3 объемов по 1 мл |
нижний |
верхний |
|
|
1 |
2 |
3 |
4 |
5 |
6 |
|
0 |
0 |
1 |
0,3 |
0 |
1,4 |
|
0 |
0 |
2 |
* |
||
|
_______________
|
|||||
|
0 |
0 |
3 |
* |
||
|
0 |
1 |
0 |
0,3 |
0,1 |
1,4 |
|
0 |
1 |
1 |
* |
||
|
0 |
1 |
2 |
* |
||
|
0 |
1 |
3 |
* |
||
|
0 |
2 |
0 |
0,6 |
0,1 |
2,8 |
|
0 |
2 |
1 |
* |
||
|
0 |
2 |
2 |
* |
||
|
0 |
2 |
3 |
* |
||
|
0 |
3 |
0 |
* |
||
|
0 |
3 |
1 |
* |
||
|
0 |
3 |
2 |
* |
||
|
0 |
3 |
3 |
* |
||
|
1 |
0 |
0 |
0,4 |
0,1 |
1,7 |
|
1 |
0 |
0 |
0,7 |
0,2 |
3,4 |
|
1 |
0 |
2 |
* |
||
|
1 |
0 |
3 |
* |
||
|
1 |
1 |
0 |
0,7 |
0,2 |
3,4 |
|
1 |
1 |
1 |
1,1 |
0,2 |
5,2 |
|
1 |
1 |
2 |
* |
||
|
1 |
1 |
3 |
* |
||
|
1 |
2 |
0 |
1,1 |
0,2 |
5,3 |
|
1 |
2 |
1 |
* |
||
|
1 |
2 |
2 |
* |
||
|
1 |
2 |
3 |
* |
||
|
1 |
3 |
0 |
* |
||
|
1 |
3 |
1 |
* |
||
|
1 |
3 |
2 |
* |
||
|
1 |
3 |
3 |
* |
||
|
2 |
0 |
0 |
0,9 |
0,2 |
4,3 |
|
2 |
0 |
1 |
1,4 |
0,3 |
6,7 |
|
2 |
0 |
2 |
* |
||
|
2 |
0 |
3 |
* |
||
|
2 |
1 |
0 |
1,5 |
0,3 |
6,9 |
|
2 |
1 |
1 |
2 |
0,4 |
9,6 |
|
2 |
1 |
2 |
* |
||
|
2 |
1 |
3 |
* |
||
|
2 |
2 |
0 |
2 |
0,5 |
9,9 |
|
2 |
2 |
1 |
3 |
0,6 |
12,9 |
|
2 |
2 |
2 |
* |
||
|
2 |
2 |
3 |
* |
||
|
2 |
3 |
0 |
3 |
0,6 |
13,3 |
|
2 |
3 |
1 |
* |
||
|
2 |
3 |
2 |
* |
||
|
2 |
3 |
3 |
* |
||
|
3 |
0 |
0 |
2 |
0,5 |
10,8 |
|
3 |
0 |
1 |
4 |
0,8 |
18,0 |
|
3 |
0 |
2 |
6 |
1,4 |
29,7 |
|
3 |
0 |
3 |
* |
||
|
3 |
1 |
0 |
4 |
0,9 |
20,0 |
|
3 |
1 |
1 |
8 |
1,6 |
35,0 |
|
3 |
1 |
2 |
12 |
2,5 |
53,8 |
|
3 |
1 |
3 |
* |
||
|
3 |
2 |
0 |
9 |
2,0 |
43,6 |
|
3 |
2 |
1 |
15 |
3,2 |
69,8 |
|
3 |
2 |
2 |
21 |
4,6 |
100,3 |
|
3 |
2 |
3 |
29 |
6,2 |
136,4 |
|
3 |
3 |
0 |
24 |
5,1 |
112,1 |
|
3 |
3 |
1 |
46 |
9,3 |
216,0 |
|
3 |
3 |
2 |
110 |
23,5 |
516,6 |
|
3 |
3 |
3 |
|
- |
- |
Таблица 1.2
Расчет наиболее вероятного числа (НВЧ) колифагов в 100 мл
Наиболее вероятное число (НВЧ) в 100 мл
|
Число положительных результатов |
НВЧ в 100 мл |
Вероятность |
Нижний предел |
Верхний предел |
|
|
из 1 объема по 50 мл |
из 5 объемов по 10 мл |
||||
|
1 |
4 |
16,1 |
0,4095 |
1,9 |
113,9 |
|
1 |
3 |
9,3 |
0,3422 |
1,1 |
77,4 |
|
1 |
2 |
5,6 |
0,3218 |
0,7 |
46,4 |
|
1 |
1 |
3,2 |
0,3039 |
0,4 |
26,2 |
|
1 |
0 |
1,4 |
0,2500 |
0,2 |
11,5 |
|
0 |
5 |
6,9 |
0,0010 |
0,8 |
57,6 |
|
0 |
4 |
5,1 |
0,0060 |
0,6 |
42,5 |
|
0 |
3 |
3,6 |
0,0222 |
0,4 |
29,6 |
|
0 |
2 |
2,2 |
0,0671 |
0,3 |
18,5 |
|
0 |
1 |
1,1 |
0,1937 |
0,1 |
8,8 |
Приложение 2
(обязательное)
Ведение эталонных культур
Ведение эталонных культур обеспечивает максимальное сохранение типовых свойств штаммов, что достигается соблюдением принципов их культивирования, контроля и хранения.
Согласно санитарным правилам СП 1.2.036-95 "Порядок учета, хранения, передачи и транспортирования микроорганизмов III-IV групп патогенности", п.3.1.6 "Производственным предприятиям, контролирующим готовую продукцию, разрешается иметь только коллекцию типовых культур, предусмотренных нормативно-технической документацией".
Хранение культур осуществляется в соответствии с п.3.2.12 СП 1.2.036-95. Лаборатория должна иметь разрешение на работу с микроорганизмами III-IV групп патогенности.
1. Ведение бактериальных культур аэробов и факультативных анаэробов
Основные положения
В качестве контрольных тест-штаммов используют эталонные культуры, полученные из официально признанной коллекции микроорганизмов (п.4.5).
Хранение запасов рабочей культуры осуществляется в столбике полужидкого агара, срок хранения 3 мес.
Для целевого использования пригодна суточная ("ночная") культура эталонного штамма, прошедшая не более 2 пассажей на питательных средах, с момента высева со среды для хранения запасов рабочей культуры.
Восполнение запасов рабочей культуры допускается не более трех раз. В этой связи срок использования эталонной культуры с момента вскрытия ампулы - 1 год.
На этапах восстановления из лиофилизированного состояния и восполнения запасов рабочих культур осуществляется контроль сохранения видовых и паспортных свойств тест-культуры.
Культура с измененными свойствами в анализе не используется.
По истечении года необходимо получить новую лиофилизированную эталонную культуру из коллекции микроорганизмов.
Процедура ведения культуры включает следующие этапы:
- восстановление лиофилизированной культуры;
- создание и хранение запасов рабочей культуры;
- восполнение запасов рабочей культуры;
- подготовка культуры для целевого использования в анализе;
- контроль видовых и паспортных свойств.
1.1. Восстановление лиофилизированной эталонной культуры
Оттянутый конец ампулы с лиофилизированной культурой нагревают над пламенем горелки. Влажным концом стерильного ватного тампона прикасаются к нагретой части, в результате чего появляются трещины. Конец ампулы накрывают трехслойной марлевой салфеткой, смоченной 70°-ным этиловым спиртом и хорошо отжатой, и обламывают пинцетом.
После вскрытия ампула остается накрытой той же салфеткой в течение (1-2) мин. Затем салфетку осторожно снимают и вместе с остатками стекла погружают в дезраствор. В ампулу вносят 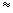 0,5 мл питательного бульона (п.5.2.1) для регидратации. Содержимое ампулы перемешивают, переносят стерильной пастеровской пипеткой или шприцем в пробирку с питательным бульоном и инкубируют при (37±1) °С в течение 18-24 ч.
0,5 мл питательного бульона (п.5.2.1) для регидратации. Содержимое ампулы перемешивают, переносят стерильной пастеровской пипеткой или шприцем в пробирку с питательным бульоном и инкубируют при (37±1) °С в течение 18-24 ч.
После инкубации из питательного бульона делают высев петлей на скошенный питательный агар в две пробирки (п.5.3.1).
При восстановлении штамма E. coli К12 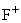
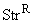 посев осуществляется на скошенный питательный агар, содержащий стрептомицин (п.5.3.5).
посев осуществляется на скошенный питательный агар, содержащий стрептомицин (п.5.3.5).
Посевы инкубируют при 37 °С в течение (18-24) ч.
Одну пробирку с посевом используют для постановки тестов на соответствие полученного штамма видовым, паспортным свойствам (п.п.1.5.2-1.5.5 приложения 2).
Второй посев на скошенном питательном агаре используют для создания запасов рабочей культуры (п.1.2 приложения 2).
Оставшуюся бульонную культуру E. coli М17-02 используют для оценки степени диссоциации эталонного штамма, как это описано в пункте 1.5.1 приложения 2.
При несоответствии штамма видовым и паспортным свойствам и (или) при наличии более 25% полиморфных (нетипичных) колоний в R-форме полученную культуру для работы не используют.
1.2. Создание запасов рабочей культуры
При удовлетворительном прохождении контрольных тестов (п.п.1.5.1-1.5.5 приложения 2) культуру со скошенного питательного агара (для E. coli К12 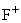
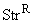 - с питательного агара со стрептомицином) засевают уколом в столбик с полужидким агаром (п.5.3.4). В зависимости от интенсивности работы лаборатории посев проводят в 4-10 пробирок, из расчета по 1-3 пробирки на 1 мес. работы и 1 пробирки для восполнения запасов рабочей культуры через 3 мес. на следующий квартал (п.1.3 приложения 2).
- с питательного агара со стрептомицином) засевают уколом в столбик с полужидким агаром (п.5.3.4). В зависимости от интенсивности работы лаборатории посев проводят в 4-10 пробирок, из расчета по 1-3 пробирки на 1 мес. работы и 1 пробирки для восполнения запасов рабочей культуры через 3 мес. на следующий квартал (п.1.3 приложения 2).
Посевы инкубируют (18-24) ч при 37 °С. При наличии роста пробирки закрывают резиновыми (силиконовыми) пробками и закладывают на хранение при температуре (4-8) °С.
Одну из пробирок с культурой, предназначенной для восполнения рабочих запасов, маркируют и хранят отдельно. Запасы рабочей культуры желательно хранить в отдельном холодильнике.
1.3. Восполнение запасов рабочей культуры
Восполнение запасов рабочей культуры производится в конце третьего, шестого и девятого месяца с момента вскрытия ампулы (каждые 3 мес.).
Для восполнения запасов рабочей культуры используется субкультура на среде хранения, полученная ранее при создании запасов или при очередном их восполнении.
Из пробирки с культурой, предназначенной для восполнения запасов, производят посев в питательный бульон. Посевы инкубируют при 37 °С (18-24) ч.
После инкубации из питательного бульона делают высев петлей в две пробирки со скошенным питательным агаром (п.5.3.1). При ведении штамма E. coli К12 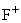
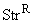 посев осуществляется на скошенный питательный агар, содержащий стрептомицин (5.3.5). Посевы инкубируют при 37 °С (18±2) ч.
посев осуществляется на скошенный питательный агар, содержащий стрептомицин (5.3.5). Посевы инкубируют при 37 °С (18±2) ч.
Один из посевов используют для постановки тестов на соответствие полученного штамма видовым, паспортным свойствам (п.п.1.5.2-1.5.5 приложения 2).
Второй посев на скошенном питательном агаре используют для восполнения запасов рабочей культуры (п.1.2 приложения 2).
Оставшуюся бульонную культуру E. coli М17-02 используют для оценки степени диссоциации эталонного штамма, как это описано в п.1.5.1 приложения 2.
При наличии более 25% полиморфных (нетипичных) колоний и (или) при несоответствии штамма видовым и паспортным свойствам полученную культуру для дальнейшей работы не используют.
Необходимо получить новую ампулу с эталонной культурой и начать процедуру ведения тестового штамма сначала.
При удовлетворительном прохождении контрольных тестов процедура закладки культуры на хранение осуществляется согласно п.1.2 приложения 2.
Восполнение запасов рабочей культуры проводят только три раза.
По истечении года использования необходимо получить новую эталонную культуру из коллекции микроорганизмов.
1.4. Подготовка культуры для целевого использования в анализе
Накануне использования культуру с полужидкого агара высевают на 2 пробирки со скошенным питательным агаром (п.5.3.1). Для культуры E. coli К12 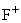
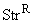 используют питательный агар со стрептомицином (п.5.3.5). Посев инкубируют (18-24) ч при 37 °С.
используют питательный агар со стрептомицином (п.5.3.5). Посев инкубируют (18-24) ч при 37 °С.
Культуру из одной пробирки используют по назначению. Вторая пробирка с культурой на скошенном питательном агаре используется для получения культуры для работы на следующий (второй) день.
При необходимости получения культуры тест-штамма на третий день высев снова производят с полужидкого агара.
1.5. Контроль эталонных бактериальных культур
Постановка контроля включает:
-
оценку степени диссоциации культуры E. coli М17-02;
-
проверку видовых свойств бактериальных культур;
-
проверку способности E. coli К12
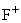
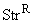 проверку культуры E. coli К12
проверку культуры E. coli К12 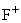
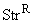 на однородность и отсутствие загрязнения фагом.
на однородность и отсутствие загрязнения фагом.
1.5.1. Оценка степени диссоциации культуры E. coli М 17-02
Из 18-часовой бульонной культуры делают 10-кратные разведения физиологическим раствором. По 0,1 мл из 5 и 6 разведения засевают на 2 чашки питательного агара предварительно подсушенные в термостате. Шпателем посевы распределяют по поверхности агара до полного исчезновения влаги и инкубируют в термостате при температуре (37±1) °С в течение (18-24) ч.
Выбирают чашки, на которых выросло от 30 до 100 колоний.
Проверку тест-штаммов на диссоциацию производят путем визуального просмотра изолированных колоний на чашках в прямом и косонаправленном свете через бинокулярную лупу или микроскоп на малом увеличении.
На питательном агаре бактерии вида E. coli образуют колонии средней величины (3-5) мм, плоско-выпуклые, круглые, гладкие с ровным краем (S-форма), влажные, блестящие, прозрачные в прямом и непрозрачные (опалово-мутные) в косопроходящем свете. В косопроходящем свете колонии эшерихий могут иметь равномерную зернистость.
В R-форме колонии эшерихий более плоские, большего размера, неправильной формы с неровными краями и шероховатой, матовой поверхностью.
При наличии диссоциации (по размеру, S-R-диссоциация, др.) подсчитывают количество измененных колоний и общее количество просмотренных колоний. Общее количество просмотренных бактерий не должно быть менее 30. Затем рассчитывают процент диссоциации по формуле:

Если процент диссоциированных колоний более 25%, то данная культура не пригодна для дальнейшего использования.
1.5.2. Контроль видовых свойств E. coli М17-02 и E. coli К12 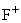
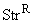
После восстановления лиофилизированной культуры проводится типирование культуры по биохимическим свойствам до вида.
Идентификацию рекомендуется проводить с использованием тест-систем биохимической идентификации семейства Enterobacteriaceae, разрешенных к применению. При этом следует руководствоваться рекомендациями производителя. Правомочна постановка отдельных биохимических тестов.
Перед очередным ежеквартальным созданием запаса рабочей культуры оценку эталонного штамма E. coli проводят путем подтверждения следующих основных свойств:
- отсутствие оксидазной активности;
- грам-негативности;
- способности образовывать на среде Эндо характерные темно-красные (малиновые) колонии с металлическим блеском и отпечатком на среде;
- способности утилизировать лактозу до кислоты и газа при температуре 37 °С в течение 24-48 ч и 44 °С в течение 24 ч;
- способности утилизировать глюкозу до кислоты и газа при температуре 37 °С в течение 24 ч.
Если культура не соответствует видовым свойствам, то она не пригодна для дальнейшего использования.
1.5.3. Проверка чувствительности E. coli К12 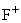
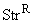
Способность E. coli К12 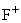
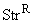 лизироваться специфичным фагом, является основополагающим свойством тест-культуры, на котором основан метод определения колифагов в воде.
лизироваться специфичным фагом, является основополагающим свойством тест-культуры, на котором основан метод определения колифагов в воде.
Проверка чувствительности осуществляется каждый раз, когда из запасов хранения берется новая пробирка с рабочей культурой, хранящейся на полужидком агаре.
Выполнение анализа
Бактериальную взвесь готовят по п.8.5.2.3. На 100 мл расплавленного и остуженного до (45-49) °С питательного агара вносят 1 мл бактериальной взвеси и разливают в чашки. После застывания чашки на поверхность агара наносят каплю (0,05 мл) суспензии фага, не захватывая хлороформа. Инкубируют в течение 18-24 ч при 37 °С. Просмотр посевов следует осуществлять в проходящем свете.
Культура считается восприимчивой и пригодной для проведения анализов воды при наличии четких зон лизиса. При отсутствии зон лизиса культура не пригодна для использования и подлежит замене.
1.5.4. Проверка культуры E. coli К12 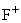
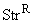 на загрязненность фагом
на загрязненность фагом
Бактериальную взвесь готовят по п.8.5.2.3, вносят в расплавленный и остуженный до температуры (45-49) °С питательный агар из расчета 1 мл взвеси на 100 мл агара. Чашку Петри заливают приготовленной смесью, инкубируют при температуре 37 °С (18-24) ч.
Просмотр посевов осуществляют в проходящем свете. Культура должна давать равномерный газон роста. Наличие зон лизиса в контроле свидетельствует о загрязненности культуры фагами.
1.5.5. Контроль видовых свойств Pseudomonas aeruginosa и Pseudomonas fluorescens
Оценку эталонного штамма Pseudomonas aeruginosa и Pseudomonas fluorescens проводят путем подтверждения следующих свойств:
- наличия оксидазной активности;
- грам-негативности;
- роста на ПБ в виде серебристой пленки на поверхности с образованием кольца сине-зеленого пигмента;
- наличия сине-зеленого пигмента пиоцианина при росте на ПА при 37 °С;
- способности роста на питательном агаре при 42 °С в течение 24 ч (для Pseudomonas aeruginosa);
- способности роста на питательном агаре при 4 °С в течение 24 ч (для Pseudomonas fluorescens).
Если культура не соответствует видовым свойствам, то она не пригодна для дальнейшего использования.
2. Культивирование, хранение и контроль эталонных культур бактериофагов
В качестве эталонного штамма для проведения контроля культуры клеток-хозяина при проведении анализа на колифаги используется РНК-содержащий фаг MS2.
Процесс ведения эталонного штамма колифага MS2 состоит из 2 функциональных блоков:
- восстановление лиофилизированной культуры;
- создание запасов эталонной культуры и культур для целевого использования.
2.1. Восстановление лиофилизированной культуры
Оттянутый конец ампулы с лиофилизированными культурами нагревают над пламенем горелки. Влажным концом стерильного ватного тампона прикасаются к нагретой части, в результате чего появляются трещины.
Конец ампулы накрывают трехслойной марлевой салфеткой, смоченной 70°-ным этиловым спиртом и хорошо отжатой, и обламывают пинцетом.
После вскрытия ампула остается накрытой той же салфеткой в течение (1-2 мин). Затем салфетку осторожно снимают и вместе с остатками стекла погружают в дезраствор. В ампулу вносят  0,5 мл питательного бульона для регидратации.
0,5 мл питательного бульона для регидратации.
2.2. Создание запасов эталонных культур фага и культур для целевого использования
Рабочую культуру E. coli К12 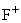
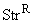 , хранящуюся на полужидком агаре, засевают в пробирку с 10 мл питательного бульона. Посевы инкубируют при (37±1) °С (18-24) ч.
, хранящуюся на полужидком агаре, засевают в пробирку с 10 мл питательного бульона. Посевы инкубируют при (37±1) °С (18-24) ч.
После инкубации 0,1 мл полученной бульонной культуры повторно засевают в 3-4 пробирки с 10 мл питательного бульона и помещают в термостат при (37±1) °С. Через 2 час инкубации в каждую пробирку вносят регидрированную культуру фага 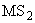 *, инкубацию продолжают до (18-24) ч. После инкубации в пробирку добавляют по 1 мл хлороформа, герметично укупоривают, интенсивно встряхивают и оставляют на ночь в холодильнике.
*, инкубацию продолжают до (18-24) ч. После инкубации в пробирку добавляют по 1 мл хлороформа, герметично укупоривают, интенсивно встряхивают и оставляют на ночь в холодильнике.
_________________
* Текст соответствует оригиналу.
Пипеткой отбирают бульон над осевшим хлороформом и переносят в стерильные пробирки, добавляют по 1 мл хлороформа, герметично укупоривают, встряхивают и хранят в холодильнике.
Одну пробирку используют для целевого назначения в контроле чувствительности культуры E. coli К12 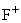
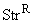 к фагу. Две других служат запасом эталонного фага.
к фагу. Две других служат запасом эталонного фага.
Активность полученной культуры определяется титром фага. Для использования допускается культура с титром более 10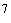 -10
-10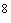 . Через год хранения титр фага может снизиться. В этой связи необходимо получить новую культуру или провести определение титра хранящегося фага.
. Через год хранения титр фага может снизиться. В этой связи необходимо получить новую культуру или провести определение титра хранящегося фага.
2.3. Определение титра фага
Для определения титра фага выполняется серия десятикратных разведений культуры фага (п.2.2). По 1 мл каждого разведения вносят в чашки Петри и заливают смесью питательного агара и E. coli К12 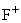
 , приготовленной аналогично описанному в п.1.5.4 приложения 2. Посевы инкубируют при (37±1) °С. Пробирки с разведениями закупоривают резиновыми или силиконовыми пробками и хранят до получения результатов при температуре (4±2) °С для приготовления рабочих суспензий фага.
, приготовленной аналогично описанному в п.1.5.4 приложения 2. Посевы инкубируют при (37±1) °С. Пробирки с разведениями закупоривают резиновыми или силиконовыми пробками и хранят до получения результатов при температуре (4±2) °С для приготовления рабочих суспензий фага.
Через (18-24) ч инкубации просчитывают количество бляшек на чашках. Учету подлежат чашки, на которых отмечается рост 30-100 негативных колоний фага.
При получении титра менее 10 фаг можно размножить. Для нарастания титра необходимо повторить описанную процедуру.
фаг можно размножить. Для нарастания титра необходимо повторить описанную процедуру.
После выполнения работ с культурами фагов необходимо провести тщательную обработку помещения дезсредствами и обеззараживание ультрафиолетовым облучением.
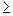 240
240