МР 11-3/278-09 Методы выявления бактерий рода Salmonella в пищевых продуктах с использованием анализатора Vidas/miniVidas производства фирмы "BioMerieux", Франция
МР 11-3/278-09
МЕТОДИЧЕСКИЕ РЕКОМЕНДАЦИИ
Методы выявления бактерий рода 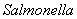 в пищевых продуктах с использованием анализатора Vidas/miniVidas производства фирмы "BioMerieux", Франция
в пищевых продуктах с использованием анализатора Vidas/miniVidas производства фирмы "BioMerieux", Франция
Дата введения 2001-09-20
1. РАЗРАБОТАНЫ: Федеральным центром Госсанэпиднадзора Минздрава России (Подунова Л.Г., Минаева Н.А., Кривопалова Н.С.) при участии фирмы "BioMerieux", Франция (Мурзак О.А.).
2. УТВЕРЖДЕНЫ И ВВЕДЕНЫ В ДЕЙСТВИЕ заместителем Главного государственного санитарного врача Российской Федерации - Руководителем Департамента госсанэпиднадзора Минздрава России С.И.Ивановым 20 сентября 2001 г.
3. ВВЕДЕНЫ ВПЕРВЫЕ
1. Общие положения и область применения
1.1. Настоящие методические рекомендации устанавливают методы проведения лабораторных исследований по выявлению бактерий рода Salmonella в пищевых продуктах и продовольственном сырье с использованием автоматического анализатора Vidas/miniVidas.
1.2. Методические рекомендации разработаны в соответствии с Федеральным законом "О санитарно-эпидемиологическом благополучии населения", Положением о государственном санитарно-эпидемиологическом нормировании, Положением о государственной санитарно-эпидемиологической службе Российской Федерации.
1.3. Методические рекомендации предназначены для применения в лабораториях организаций, независимо от форм собственности, осуществляющих производственный контроль продовольственного сырья и пищевых продуктов в процессе промышленного производства и выпуска продукции; в лабораториях учреждений государственной санитарно-эпидемиологической службы Российской Федерации и санитарно-эпидемиологической службы федеральных органов исполнительной власти, осуществляющих государственный и ведомственный контроль, гигиеническую оценку и выдачу санитарно-эпидемиологических заключений, а также в лабораториях других организаций, аккредитованных в установленном порядке на право проведения контроля качества пищевой продукции и продовольственного сырья для целей сертификации, в т.ч. импортируемых в Российскую Федерацию.
2. Нормативные ссылки
2.1. Федеральный закон "О санитарно-эпидемиологическом благополучии населения" N 52-ФЗ от 30 марта 1999 г.
2.4. Положение о государственной санитарно-эпидемиологической службе Российской Федерации, утвержденное постановлением Правительства Российской Федерации N 554 от 24 июля 2000 г.
2.5. Положение о государственном санитарно-эпидемиологическом нормировании, утвержденное постановлением Правительства Российской Федерации N 554 от 24 июля 2000 г.
2.6. СП 1.2.731-99* "Безопасность работы с микроорганизмами III-IV групп патогенности и гельминтами".
______________
* На территории Российской Федерации документ не действует. Действуют СП 1.3.2322-08, здесь и далее по тексту. - Примечание изготовителя базы данных.
2.7. СанПиН 2.3.2.560-96* "Гигиенические требования к качеству и безопасности продовольственного сырья и пищевых продуктов".
______________
* На территории Российской Федерации документ не действует. Действуют СанПиН 2.3.2.1078-01, здесь и далее по тексту. - Примечание изготовителя базы данных.
2.8. ГОСТ 26668-85 "Продукты пищевые и вкусовые. Порядок отбора проб для микробиологических анализов".
2.9. ГОСТ 26669-85 "Продукты пищевые и вкусовые. Подготовка проб для микробиологических анализов".
2.10. ГОСТ Р 50480-96* "Продукты пищевые. Метод выявления бактерий рода Salmonella".
_______________
* Вероятно ошибка оригинала. Следует читать: ГОСТ Р 50480-93. На территории Российской Федерации документ не действует. Действует ГОСТ Р 52814-2007, здесь и далее по тексту. - Примечание изготовителя базы данных.
2.11. ГОСТ 26670-91 "Продукты пищевые. Методы культивирования микроорганизмов".
2.12. ГОСТ Р 51446-99* (ИСО 7218-96) "Микробиология. Продукты пищевые. Общие правила микробиологических исследований".
______________
* На территории Российской Федерации документ не действует. Действует ГОСТ Р ИСО 7218-2008, здесь и далее по тексту. - Примечание изготовителя базы данных.
3. Требования к помещениям
3.1. Общее расположение лаборатории, а также ее инфраструктура должны удовлетворять требованиям СП 1.2.731, по ГОСТу Р 51446.
3.2. Лаборатория должна иметь разрешение на работу с микроорганизмами III-IV групп патогенности.
4. Аппаратура, питательные среды, реактивы, диагностические сыворотки, контрольные штаммы
4.1. Средства измерения
4.1.1. Автоматический иммуноферментный анализатор Vidas/miniVidas фирмы "BioMerieux", Франция.
4.1.2. Автоматический пипеточный дозатор с одноразовыми наконечниками, объемом от 100 до 1000 мкл.
|
4.1.3. Весы лабораторные общего назначения, 2-го и 4-го класса точности с наибольшим пределом взвешивания 200 г (или получаемые по импорту) |
_______________
* На территории Российской Федерации документ не действует. Действует ГОСТ Р 53228-2008. - Примечание изготовителя базы данных.
4.2. Испытательное оборудование
|
4.2.1. Аппарат универсальный для встряхивания жидкости в колбах и пробирках (или другая аппаратура для встряхивания) |
ТУ 64-1-2451-78* |
|
|
________________ * ТУ, упомянутые здесь и далее по тексту, являются авторской разработкой. За дополнительной информацией обратитесь по ссылке. - Примечание изготовителя базы данных. |
||
|
4.2.2. Водяная баня с терморегулятором, позволяющая поддерживать температуру от 0 до 100 °С |
ТУ 42-22-608-75 |
|
|
4.2.3. Термостат электрический, позволяющий поддерживать температуру 15-65 °С с отклонением от заданной ±1 °С |
ТУ 64-1-1382-83 |
|
|
4.2.4. Стерилизатор паровой медицинский или аналогичный |
ГОСТ 19569-89* |
|
_______________
* На территории Российской Федерации документ не действует. Действует ГОСТ Р 51935-2002. - Примечание изготовителя базы данных.
4.2.5. Гомогенизатор бактериологический перистальтического типа со стерильными пластиковыми пакетами (или других видов, выдерживающих условия стерилизации).
4.3. Вспомогательное оборудование
|
4.3.1. Холодильник бытовой электрический |
||
|
4.3.2. Облучатель бактерицидный настенный ОБН-150 (или других видов) |
ТУ 16-535-84 |
4.4. Питательные среды и реактивы*
________________
* Питательные среды и биохимические препараты имеют международные сертификаты качества ИСО 9.000.
|
4.4.1. Неселективный ICS бульон для развития сальмонелл после процедуры иммунного обогащения Vidas ICS, готовый к использованию (в пробирках по 2 мл) |
Cat. N 42 610 |
|
|
4.4.2. Пептонная вода забуференная - разбавитель для приготовления суспензий при определении бактерий рода Salmonella (готовая или в сухом виде): |
||
|
готовая во флаконах по 225 мл |
Cat. N 42 043 |
|
|
готовая во флаконах по 90 мл |
Cat. N 42 042 |
|
|
в сухом виде для приготовления по способу, указанному в каталоге питательных сред |
Cat. N 51 094 |
|
|
4.4.3. Среда Раппапорт-Василиадис - бульон для селективного накопления, готовая к использованию (в пробирках по 10 мл) |
Cat. N 42 073 |
|
|
4.4.4. Среда Бульон М для обогащения сальмонелл, готовая к использованию (в пробирках по 10 мл) |
Cat. N 42 077 |
|
|
4.4.5. Среда Селенит-цистиновый бульон, готовая к использованию (в пробирках по 10 мл) |
Cat. N 42 052 (фирма "BioMerieux", Франция) |
|
|
4.4.6. SM ID селективная хромогенная среда для прямой идентификации бактерий рода Salmonella (готовая или в сухом виде): |
||
|
готовая (в чашках диаметром 90 мм) |
Cat. N 43 291 (фирма "BioMerieux", Франция) |
|
|
в сухом виде для приготовления по способу, указанному в каталоге питательных сред |
Cat. N 43 291 (фирма "BioMerieux", Франция) |
|
|
4.4.7. Среда Hektoen enteric агар-среда для селективного выделения микроорганизмов рода Salmonella (готовая или в сухом виде): |
||
|
готовая (в чашках диаметром 90 мм) |
Cat. N 43 111 |
|
|
в сухом виде для приготовления по способу, указанному в каталоге питательных сред |
Cat. N 51 050 |
|
|
4.4.8. Среда Висмут-сульфитный агар для селективного выделения микроорганизмов рода Salmonella - в сухом виде для приготовления по способу, указанному в каталоге питательных сред |
Cat. N 51 065 (фирма "BioMerieux", Франция) |
|
|
4.4.9. Среда XLD-агар для выделения патогенных кишечных бактерий (готовая или в сухом виде): |
||
|
готовая (в чашках диаметром 90 мм) |
Cat. N 43 563 |
|
|
в сухом виде для приготовления по способу, указанному в каталоге питательных сред |
Cat. N 51 049 |
|
|
4.4.10. Набор Vidas ICS* |
Cat. N 30 435 |
|
________________
* Условия хранения, срок годности, использование набора Vidas ICS в соответствии с инструкциями изготовителя.
в составе:
4.4.10.1. ICS стрип с готовыми к использованию набором реактивов, состоящий из 10 лунок:
-
1-я лунка - для иммуноконцентрированного раствора;
-
2-я лунка - нейтрализующий раствор: TРИС-HCI-буфер (рН=7,7) + твин;
-
3-я лунка - разделяющий раствор: ацетат натрия + фермент;
-
4-я лунка - для образца;
-
5-я, 7-я, 8-я, 9-я лунки - растворы для промывания: ТРИС-NaCI-буфер (150 мМ/л, рН=7,6) + твин +0,5 г/л азида натрия;
-
6-я лунка - раствор для предварительного промывания: MOPS (480 мМ/л, рН=7,8) + твин +0,5 г/л азида натрия;
-
10-я лунка - субстрат: 4-метил-умбеллиферил фосфат +1 г/л азида натрия (для измерения стандарта).
4.4.10.2. ICS-конус с твердой фазой используется как пипетирующее устройство. Внутренняя поверхность конуса покрыта антителами к сальмонеллам (к жгутиковому и соматическому антигену).
4.4.10.3. Стандарт (во флаконе по 6 мл) - поликлональные антитела коньюгированные с щелочной фосфатазой + 1 г/л азида натрия + белковый стабилизатор.
|
4.4.11. Набор Vidas SLM* |
Cat. N 30 702 |
________________
* Условия хранения, срок годности, использование набора Vidas SLM в соответствии с инструкциями изготовителя.
в составе:
4.4.11.1. Стрип SLM с готовыми к использованию набором реактивов для промывания и разделения, состоящий из 10 лунок:
-
1-я лунка - для обогащенного прокипяченного образца;
-
2-я лунка - раствор для предварительного промывания: TBS-твин +1 г/л азида натрия;
-
3-я, 4-я, 5-я, 7-я, 8-я, 9-я лунки - растворы для промывания: TBS-твин +1 г/л азида натрия;
-
6-я лунка - коньюгат: щелочная фосфатаза коньюгированная с поликлональными антителами +1 г/л азида натрия;
-
10-я лунка - оптическая кювета с субстратом: 4-метилумбеллиферил фосфат +1 г/л азида натрия;
-
4.4.11.2. SLM-конус с твердой фазой используется как пипетирующее устройство. Внутренняя поверхность конуса покрыта антителами к сальмонеллам.
4.4.11.3. Стандарт (во флаконе по 6 мл) - очищенный, инактивированный антиген сальмонелл с 1 г/л азида натрия и белковым стабилизатором.
4.4.11.4. Положительный контроль (во флаконе по 6 мл) - очищенный, инактивированный антиген сальмонелл с 1 г/л азида натрия и белковым стабилизатором.
4.4.11.5. Отрицательный контроль (во флаконе по 6 мл) - ТРИС-буфер (TBS) - твин с 1 г/л азида натрия.
|
4.4.12. API 20 Е - система для биохимической идентификации Enterobacteriaceae и других грамотрицательных палочек. |
Cat. N 20 100 (фирма "BioMerieux", Франция) |
4.5. Диагностические сыворотки
4.5.1. Сухие агглютинирующие адсорбированные поливалентные сальмонеллезные сыворотки основных групп А, В, С, Д, Е и редких групп.
4.6. Контрольные штаммы
4.6.1. Контрольный штамм бактерий рода Salmonella (ГИСК им. Л.А.Тарасевича).
5. Описание и принцип действия прибора
Vidas/miniVidas - мультипараметрический автоматический иммуноферментный анализатор, который включает автоматизированные процедуры иммунологического связывания, концентрации и качественного определения сальмонелл в продуктах питания*.
_________________
* Прибор зарегистрирован как изделие медицинского назначения в Государственном реестре средств измерения; имеет регистрационное удостоверение: сертификат об утверждении типа средств измерений.
Прибор работает с использованием Vidas-тестов (пп.4.4.10, 4.4.11).
Анализатор Vidas/miniVidas состоит из секций для производства анализов с индивидуальными ячейками для стрипов и конусов.
Прибор выполнен в виде двух модификаций: Vidas содержит 5 секций для производства 30 анализов одновременно; miniVidas содержит 2 секции для производства 12 анализов одновременно.
Система сама контролирует все стадии анализа; компьютерная обработка и встроенный принтер позволяют автоматически распечатывать окончательный результат, который содержит все необходимые данные об анализе и полную характеристику образца.
Применяемые в приборе высокие технологии позволяют проводить исследования с высокой чувствительностью и надежностью, исключают возможность перекрестной контаминации проб.
5.1. Процедура иммуноконцентрации сальмонелл
Процедура иммуноконцентрации сальмонелл (ICS) - это полностью автоматизированная процедура селективного накопления сальмонелл, состоящая из иммунологического связывания и специфического разделения на стрипах ICS и соответствующих им пипетирующих устройствах (конусах).
Антигены сальмонелл, находящиеся в пробах пищевых продуктов, после предварительного обогащения связываются с антителами на внутренней поверхности конуса. Несвязанные компоненты образца удаляются во время последующего этапа промывания. На последнем этапе происходит освобождение связанной сальмонеллы непосредственно в лунку стрипа.
5.2. Процедура автоматизированного определения сальмонелл
В основе качественного автоматизированного определения сальмонелл в продуктах питания лежит технология энзим-связанного иммуноферментного анализа (ELFA)*.
_________________
* Enzyme-Linked Fluorescens Immunoassay.
Исследование выполняется на стрипах SLM и соответствующих им пипетирующих устройствах (конусах).
Антигены сальмонелл, присутствующие в образце продукта, после предварительного обогащения связываются с антителами на внутренней поверхности конуса. Несвязанные компоненты удаляются последующим промыванием. Антитела, конъюгированные с щелочной фосфатазой, из лунки стрипа вносятся в конус, где связываются с антигенами сальмонелл, находящимися на поверхности конуса. Несвязанные компоненты конъюгата удаляются во время последующего этапа промывания. Флюоресцентный субстрат 4-метил-умбеллиферил фосфат вносится в конус. Щелочная фосфатаза катализирует превращения флюоресцентного субстрата в флюоресцентный продукт 4-метил-умбеллиферол. Интенсивность флюоресценции измеряется оптическим сканером Vidas.
Оптический сканер прибора измеряет флюоресценцию в оптической кювете дважды для каждого образца. Первый раз измеряется фон кюветы перед внесением в нее субстрата; второй раз измеряется интенсивность флюоресценции после внесения в конус субстрата и энзиматического превращения его в флюоресцирующий продукт на поверхности конуса. Разница величин фона кюветы и показателя интенсивности флюоресценции последнего измерения составляет относительное значение флюоресценции (RFV)* тестируемого образца.
________________
* Relative Fluorescence Value.
После завершения исследования выполняется автоматическая обработка результата.
6. Методы отбора проб
Отбор проб, сопроводительная документация, транспортирование и хранение в соответствии с ГОСТом 26668 и нормативно-технической документацией на анализируемый продукт.
7. Подготовка проб к анализу
Подготовку проб для исследований проводят в соответствии с ГОСТом 26669 и нормативно-технической документацией на анализируемый продукт, регламентирующей данный этап проведения микробиологических анализов пищевых продуктов.
8. Предварительное неселективное обогащение сальмонелл
Навеску продукта, в массе (объеме) которой предусматривается отсутствие бактерий рода Salmonella в соответствии с СанПиН 2.3.2.560 и нормативно-технической документацией на анализируемый продукт, измельчают, а потом высевают в забуференную пептонную воду (п.4.4.2).
Соотношение массы (объема) продукта и забуференной пептонной воды 1:9 по объему.
Посевы термостатируют при температуре (36±1) °С в течение (21±3) часа.
9. Выявления бактерий рода Salmonella методом иммуноконцентрации с автоматизированным определением на приборе Vidas
9.1. Сущность метода
Метод выявления сальмонелл основан на использовании прибора Vidas/miniVidas для процедуры автоматической иммуноконцентрации сальмонелл в наборе Vidas ICS после предварительного неселективного обогащения с последующим автоматизированным определением сальмонелл в наборе Vidas SLM. При положительном результате на приборе дальнейшее выделение бактерий, образующих типичные колонии на агаризованных дифференциально-диагностических средах, имеющих типичные для бактерий рода Salmonella биохимические и серологические характеристики.
Исследование пищевых продуктов методом иммуноконцентрации с автоматическим определением бактерий рода Salmonella на приборе Vidas сокращает время определения сальмонелл до 24 часов при отрицательном результате.
Схема проведения анализа приведена в приложении 1.
9.2. Методы отбора проб
Отбор проб проводят по п.6.
9.3. Подготовка проб к анализу
Подготовку проб к анализу проводят по п.7.
9.4. Предварительное неселективное обогащение
Неселективное предварительное обогащение проводят по п.8.
9.5. Порядок проведения процедуры иммуноконцентрации
9.5.1. Подготовка к процедуре
9.5.1.1. Необходимое количество компонентов набора Vidas ICS (п.4.4.10) оставить при комнатной температуре не менее 30 минут.
9.5.1.2. Стандарт перед использованием необходимо тщательно перемешать.
Тестирование стандарта необходимо для подтверждения сохранности набора при транспортировании и хранении.
Стандарт должен тестироваться в каждом наборе. Результаты тестирования хранятся в компьютере в течение 2 недель и автоматически используются для анализа результатов теста.
9.5.2. Процедура иммуноконцентрации
9.5.2.1. Внести 800 мкл культуры, полученной после инкубации по п.9.4 в 4-ую лунку для образца ICS стрипа.
9.5.2.2. Внести 800 мкл стандарта в 4-ю лунку для образца ICS стрипа.
9.5.2.3. Поместить ICS стрипы и ICS конусы в соответствующие позиции прибора.
9.5.2.4. Начать анализ, как это описано в руководстве пользователя Vidas. Полностью автоматизированный анализ завершается приблизительно через 40 минут.
9.5.2.5. После окончания анализа результаты распечатываются автоматически.
Указываются тип теста, дата и время тестирования, номер партии.
Примечание: иммуноконцетрированный образец, находящийся в ICS стрипе, должен быть использован в течение 30 минут после окончания последнего этапа процедуры иммуноконцентрации.
9.6. Селективное обогащение
ICS бульон (п.4.4.1) предварительно прогреть в термостате при температуре (41±1) °С в течение 30 минут.
9.6.1. Перенести 400 мкл иммуноконцетрированного образца (п.9.5.2) из 1-ой лунки стрипа ICS во флакон с 2 мл ICS бульона.
Посевы термостатируют при температуре (41±1) °С в течение 5 часов.
9.6.2. 1 мл культуры, полученной после инкубации, перенести в пробирку.
Прогреть в течение 15 минут на водяной бане при температуре 100 °С.
9.6.3. Оставшийся ICS бульон хранить в холодильнике при температуре 3-4 °С для подтверждения наличия сальмонелл при положительном результате анализа.
9.7. Порядок проведения процедуры автоматизированного определения сальмонелл
9.7.1. Подготовка к процедуре
Необходимое для анализа количество компонентов набора Vidas SLM (п.4.4.11) оставить при комнатной температуре не менее 30 минут.
9.7.1.1. Стандарт перед использованием необходимо тщательно перемешать.
Тестирование стандарта необходимо для подтверждения сохранности набора при транспортировании и хранении.
Стандарт должен тестироваться в каждом наборе. Результаты тестирования хранятся в компьютере в течение 2 недель и автоматически используются для анализа результатов теста.
Рекомендуется тестирование стандарта в 2 стрипах.
9.7.1.2. Положительный и отрицательный контроли перед использованием тщательно перемешать.
Контроли тестируются в каждом наборе. Тестирование этих контролей необходимо для занесения пределов теста в компьютер.
9.7.1.3. Ввести в прибор соответствующую информацию для создания рабочего листа.
9.7.2. Процедура автоматизированного определения сальмонелл
9.7.2.1. Внести 500 мкл прогретой на водяной бане культуры в 1-ю лунку SLM стрипа.
9.7.2.2. Внести по 500 мкл стандарта и контролей в 1-ю лунку (отдельно для каждого) SLM стрипа.
9.7.2.3. Поместить SLM стрипы и SLM конусы в соответствующие позиции прибора, которые указаны в рабочем листе.
Убедиться, что на стрипе и конусе имеются соответствующие три буквы кода данного анализа.
9.7.2.4. Начать анализ, как это указано в руководстве пользователя Vidas.
Анализ полностью автоматизирован и завершится приблизительно через 45 минут.
9.7.3. Интерпретация результатов
9.7.3.1. Интерпретация результатов зависит от пределов значения теста.
Результаты тестирования для образца и контролей сравниваются со значениями, хранящимися в памяти компьютера.
При пределах значения теста меньше или равном 0,23 результаты интерпретируются как отрицательные (Negative); при значении больше 0,23 - как положительные (Positive).
9.7.3.2. Результаты теста распечатываются. На листе с результатами указывается: номер партии, дата и время, название теста, RFV, интерпретация результата.
9.8. Выделение и идентификация культур на агаризованных дифференциально-диагностических средах
9.8.1. Положительный результат должен быть подтвержден, используя культуры, полученные после инкубации на ICS бульоне (п.9.6.3).
9.8.2. Культуры пересевают по ГОСТу 26670 на агаризованные среды по выбору: SM ID (п.4.4.6), Hektoen (п.4.4.7), Висмут-сульфитный агар (п.4.4.8) или XLD агар (п.4.4.9).
Посевы термостатируют при температуре (36±1) °С в течение 24 часов.
9.8.3. После термостатирования посевов отмечают рост колоний, характерных для бактерий рода Salmonella:
-
на среде Hektoen колонии зеленые с черным центром;
-
на среде SM ID колонии розовые;
-
на среде Висмут-сульфитный агар колонии черные с характерным металлическим блеском и пигментированием среды под колониями, а также зеленые колонии;
-
на среде XLD агар колонии красные, а также красные колонии с черным центром.
При отсутствии в посевах на дифференциально-диагностических средах характерных для бактерий рода Salmonella колоний анализ завершается.
При наличии на дифференциально-диагностических средах колоний, характерных для бактерий рода Salmonella, проводят их дальнейшее изучение.
9.9. Биохимическое подтверждение принадлежности выделенных характерных колоний к бактериям рода Salmonella
Подозрительные колонии идентифицируют с помощью API-20E-биохимического ряда для грамотрицательных бактерий (п.4.4.12) согласно прилагаемой инструкции или по ГОСТу Р 50480 (п.5.4).
9.10. Серологическое подтверждение принадлежности культур к бактериям рода Salmonella
Серологическое подтверждение принадлежности к бактериям рода Salmonella проводят с культурами, давшими типичные биохимические реакции по ГОСТу Р 50480 (п.5.6).
При определении биохимических и серологических характеристик выделенных культур в качестве контроля используют типичный по этим показателям штамм бактерий рода Salmonella (п.4.6).
9.11. Оценка результатов анализа
Результаты выявления бактерий рода Salmonella в определенной навеске продукта записывают:
9.11.1. "Бактерии рода Salmonella обнаружены в 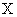 г (см
г (см ) продукта".
) продукта".
К бактериям рода Salmonella относят культуры, интерпретированные как положительные (Positive) на приборе Vidas при проведении процедуры автоматизированного определения сальмонелл, выделенные на дифференциально-диагностических средах и показавшие типичные биохимические и серологические реакции.
9.11.2. "Бактерии рода Salmonella не обнаружены в 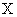 г (см
г (см ) продукта".
) продукта".
Культуры, интерпретированные как отрицательные (Negative) на приборе Vidas при проведении процедуры автоматизированного определения сальмонелл или культуры, не давшие типичных для рода Salmonella биохимических и серологических реакций.
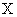 - масса (объем) навески продукта, в которой выявлены бактерии рода Salmonella.
- масса (объем) навески продукта, в которой выявлены бактерии рода Salmonella.
10. Выявление бактерий рода Salmonella методом иммуноконцентрации с выделением на агаризованных дифференциально-диагностических средах
10.1. Сущность метода
Метод выявления сальмонелл основан на использовании прибора Vidas/miniVidas для процедуры автоматической иммуноконцентрации сальмонелл в наборе Vidas ICS после предварительного неселективного обогащения с последующим выделением бактерий, образующих типичные колонии на агаризованных дифференциально-диагностических средах, имеющих типичные для бактерий рода Salmonella биохимические и серологические характеристики.
Этот метод сокращает определение сальмонелл для положительных проб до 72 часов. Метод может быть использован при высоком проценте положительных проб.
Схема проведения анализа приведена в приложении 2.
10.2. Методы отбора проб
Отбор проб проводят по п.6.
10.3. Подготовка проб к анализу
Подготовку проб к анализу проводят по п.7.
10.4. Предварительное неселективное обогащение
Предварительное неселективное обогащение проводят по п.8.
10.5. Порядок проведения процедуры иммуноконцентрации
Порядок проведения процедуры иммуноконцентрации в соответствии с п.9.5.
10.6. Выделение и идентификация культур на агаризованных дифференциально-диагностических средах
10.6.1. После процедуры иммуноконцентрации, проведенной по п.10.5, культуру из 1-ой лунки стрипа ICS стерильной петлей пересевают на агаризованные дифференциально-диагностические среды по выбору: SM ID (п.4.4.6), Hektoen (п.4.4.7), Висмут-сульфитный агар (п.4.4.8) или XLD (п.4.4.9).
10.6.2. Дальнейшую идентификацию культур проводят по пп.9.8.2, 9.8.3.
10.7. Биохимическое подтверждение принадлежности выделенных характерных колоний к бактериям рода Salmonella
Биохимическое подтверждение принадлежности характерных колоний к бактериям рода Salmonella проводят по п.9.9.
10.8. Серологическое подтверждение принадлежности культур к бактериям рода Salmonella
Серологическое подтверждение принадлежности культур к бактериям рода Salmonella проводят по п.9.10.
10.9. Оценка результатов анализа
Результаты выявления бактерий рода Salmonella в определенной навеске продукта записывают:
10.9.1. "Бактерии рода Salmonella обнаружены в 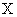 г (см
г (см ) продукта".
) продукта".
К бактериям рода Salmonella относят культуры, выделенные на дифференциально-диагностических средах, показавшие типичные биохимические и серологические реакции.
10.9.2. "Бактерии рода Salmonella не обнаружены в  г (см
г (см ) продукта".
) продукта".
Культуры, не дающие характерного для бактерий рода Salmonella роста на дифференциально-диагностических средах, не давшие типичные биохимические и серологические реакции.
 - масса (объем) навески продукта, в которой выявлены бактерии рода Salmonella.
- масса (объем) навески продукта, в которой выявлены бактерии рода Salmonella.
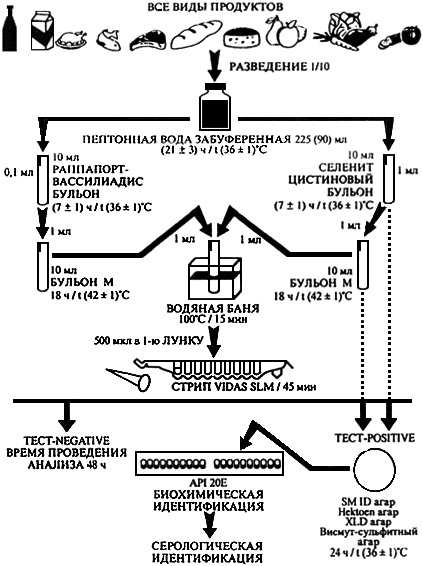
11. Автоматизированное определение сальмонелл с предварительным обогащением на селективных питательных средах
11.1. Сущность метода
Метод выявления сальмонелл основан на использовании прибора Vidas/miniVidas для процедуры автоматизированного определения сальмонелл в наборе Vidas SLM после предварительного неселективного обогащения с последующим накоплением бактерий в жидких селективных средах, выделением бактерий, образующих типичные колонии на агаризованных дифференциально-диагностических средах, имеющих типичные для бактерий рода Salmonella биохимические и серологические характеристики.
Этот метод сокращает время определения сальмонелл для отрицательных проб до 48 часов.
Схема проведения анализа приведена в приложении 3.
11.2. Методы отбора проб
Отбор проб проводят по п.6.
11.3. Подготовка проб к анализу
Подготовку проб к анализу проводят по п.7.
11.4. Предварительное неселективное обогащение
Предварительное неселективное обогащение проводят по п.8.
11.5. Селективное обогащение
11.5.1. Культуры, полученные после предварительного неселективного обогащения по п.11.4, пересевают в две среды для селективного обогащения.
Для этого 1 мл культуры перенести в пробирку с 10 мл селенит-цистиновой среды (п.4.4.5). Посевы термостатируют при температуре (36±1) °С в течение (7±1) часов.
Параллельно этому перенести 0,1 мл культуры в пробирку с 10 мл среды Раппапорт-Василиадис (п.4.4.3). Посевы термостатируют при температуре (42±1) °С в течение (7±1) часов.
11.5.2. После термостатирования перенести 1 мл селенит-цистиновой среды, в 10 мл М бульона (п.4.4.4).
В другую пробирку с 10 мл М бульона перенести 1 мл из среды Раппопорт-Василиадис.
Термостатировать обе пробирки в течение 18 часов при температуре (42±1) °С.
11.5.3. После термостатирования объединить по 1 мл культуры из каждой пробирки с М-бульоном в одну пробирку. Прогреть в течение 15 минут на водяной бане при температуре 100 °С.
11.5.4. Оставшиеся среды: Раппапорт-Василиадис, селенит-цистиновая и М-бульон хранить при температуре 3-4 °С для подтверждения положительного результата.
11.6. Автоматизированное определение сальмонелл
11.6.1. Процедуры автоматизированного определения сальмонелл проводят по п.9.7 с культурами, прогретыми на водяной бане (п.11.5.3).
11.7. Выделение и идентификация культур на агаризованных дифференциально-диагностических средах
11.7.1. Положительный результат должен быть подтвержден, используя культуры, полученные после термостатирования (п.11.5.4).
11.7.2. Дальнейшую идентификацию культур проводят по пп.9.8.2, 9.8.3.
11.8. Биохимическое подтверждение принадлежности выделенных характерных колоний к бактериям рода Salmonella
Биохимическое подтверждение принадлежности выделенных характерных колоний к бактериям рода Salmonella проводят по п.9.9.
11.9. Серологическое подтверждение принадлежности культур к бактериям рода Salmonella
Серологическое подтверждение принадлежности выделенных культур к бактериям рода Salmonella проводят по п.9.10.
11.10. Оценка результатов анализа
Оценку результатов проводят по п.9.11.
Приложение 1
Выявление бактерий рода Salmonella методом иммуноконцентрации
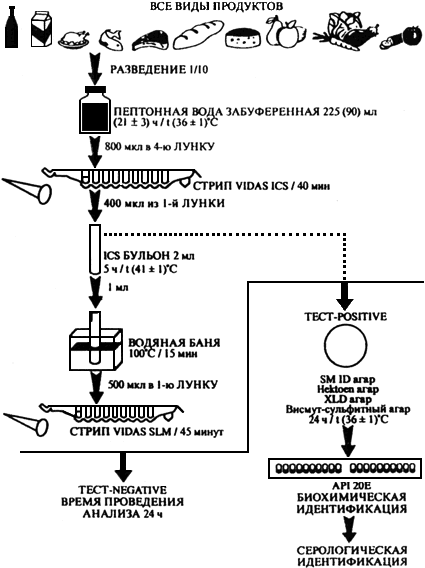
Приложение 2
Выявление бактерий рода Salmonella методом иммуноконцентрации с выделением на агаризированных дифференциально-диагностических средах
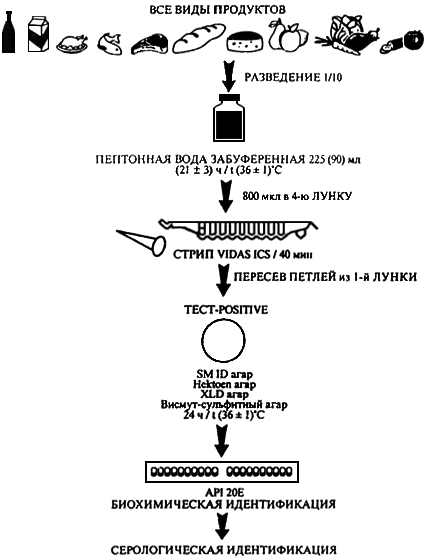
Приложение 3
Автоматизированное определение бактерий рода Salmonella с предварительным обогащением на селективных питательных средах